ответ: 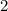 °С
°С
Объяснение:
Дано:
 °С
°С
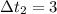 °С
°С
------------------
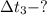
Пусть 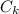 - теплоемкость калориметра
- теплоемкость калориметра
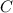 - теплоемкость воды в ложке
- теплоемкость воды в ложке
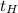 - начальная температура калориметра
- начальная температура калориметра
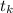 - конечная температура калориметра
- конечная температура калориметра
 - температура воды в ложке
- температура воды в ложке
Теперь запишем уравнение теплового баланса после того как мы влили первую ложку воды в пустой калориметр
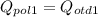
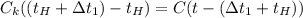
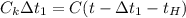 - уравнение (1)
- уравнение (1)
Аналогично и для второго случая
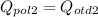
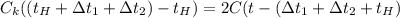
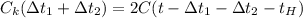 - уравнение (2)
- уравнение (2)
В уравнении (2) фигурирует 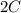 так как это уже "вторая ложка"
так как это уже "вторая ложка"
Получаем систему из уравнений (1) и (2)
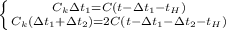
Разделим уравнение уравнение (1) на (2)
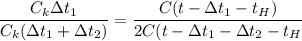
Подставляя численные значения упростим
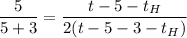
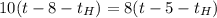
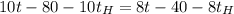
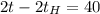
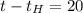 °С
°С
Тогда подставляя это в уравнение в уравнение (1) получим
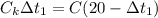
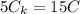
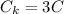
После вливания в калориметр третьей ложки получим что
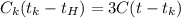
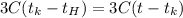
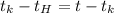
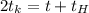
Если 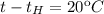 то
то 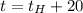
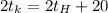
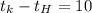 °С
°С
Допустим 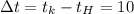 °С
°С
Тогда
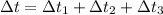
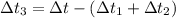
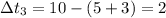 °С
°С
V=13л=0,013
РО(плотность гелия) = 0,179 кг/
Решение:
При изохорном процессе - V и m - const.
Поэтому применим закон Шарля:
1)
2) Найдем массу 13л гелия:
m=плотность*объем=0,179*0,013=0,002327кг
3) Из уравнения состояния идеального газа найдем термодинамическую температуру гелия при давлении 148000Па и объеме 13л:
T=
4) По условиям задачи Гелий нагревали и его температура возросла в 4 раза, а значит первоначальная температура была 125/4=
5) Формула для нахождения количества теплоты: Q=cm(
Q=496500 Дж