Дано:
M₁ = 28·10⁻³ кг/моль - молярная масса азота
M₂ = 44·10⁻³ кг/моль - молярная масса углекислого газа
m - масса смеси
m₁ = 0,20·m -масса азота
m₂ = 0,80·m -масса углекислого газа
T = 450 K
p = 7·10⁵ Па
ρ смеси - ?
Запишем уравнение Менделеева-Клапейрона для смеси газов:
p·V=(m₁/M₁+m₂/M₂)·R·T
p·V=m·(0,20/M₁+0,80/M₂)·R·T
Разделим обе части уравнения на объем, и учтем, что плотность:
ρ = m /V
p=ρ·(0,20/M₁+0,80/M₂)·R·T
Отсюда плотность смеси:
ρ = p /((0,20/M₁+0,80/M₂)·R·T)
ρ = 7·10⁵ /((0,20/28·10⁻³+0,80/44·10⁻³ )·8,31·450)
ρ = 7,39 кг/м³
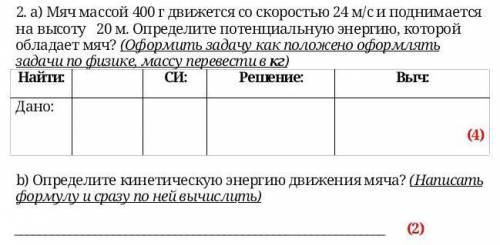
2 a)
Найти :
Еp = ?
Дано:
m = 400 г (в графе СИ 0,4 кг)
V = 24 м/с
h = 20 м
g = 10 Н/кг
Ep = mgh
Вычисления:
Ep = 0,4 кг * 10 Н/кг * 20 м = 80 Дж
b) Ек = mV^2 / 2
Eк = 0,4 кг * (24 м/с)^2 / 2 = 0,2 кг * 576 м^2/с^2 = 115,2 Дж