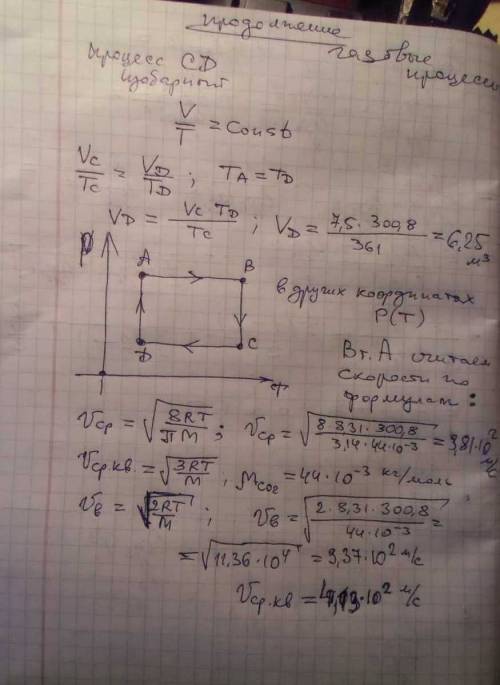
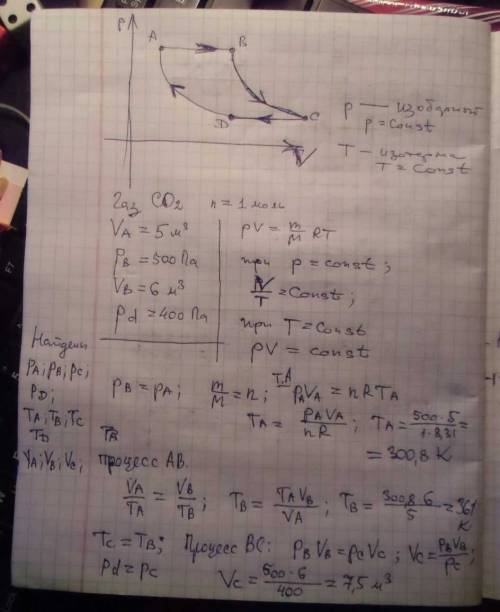
Идеальный газ меняет свое состояние по циклу abcd, состоящему из четырех последовательных процессов ав, вс, cd, da. пользуясь данными, необходимо выполнить следующее : 1) рассчитать недостающие значения р, v и т для точек а, в, с, d. нарисовать цикл в координатах, указанных в 6-ой колонке. 2) для состояния газа в точке а рассчитать среднюю арифметическую vcp, среднюю квадратичную vср.кв и наиболее вероятную vв скорости молекул. определить средние значения полной кинетической энергии w, кинетической энергии поступательного wп и кинетической энергии вращательного wвр движения молекулы. 3) для заданного в 7-ой колонке процесса записать первое начало термодинамики и рассчитать: теплоту q, подведенную к газу: изменение внутренней энергии газа δu; совершенную газом работу a, теплоемкость.