- коэффициент трансформации = 0,25
- во вторичной обмотке 2400 витков
Объяснение:
к - коэффициент трансформации, простой принцип - чем больше витков, тем больше напряжение.
То есть во сколько увеличилось напряжение на вторичной обмотке, во столько же значит больше витков во вторичной обмотке. ВСЁ.
k = 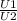 =
= 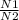
Дано:
N1 = 600 витков
U1 = 220 В
U2 = 880 В
____________
N2 - ?
k = 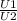
k = 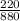 = 0,25 (коэффициент трансформации)
= 0,25 (коэффициент трансформации)
Количество витков можно решить двумя
- разделить количество витков первичной обмотки на коэффициент трансформации:
k = 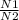
N2 = 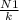 N2 =
N2 = 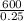 = 2400 витков
= 2400 витков
- либо можно было решить пропорцией из общей формулы:
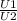 =
= 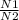
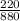 =
= 
N2 = 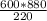 = 2400 витков
= 2400 витков


ОбъяснеРассмотрим произвольный ТП 1-2 в координатах Q=f(t), где Q – подведенная теплота в Дж, t – температура в 0С. Тогда Cm= tgα, C= tgβ.
Если ТС – однородное рабочее тело, то в расчетах применяются относительные теплоемкости:
- удельная теплоемкость – теплоемкость, отнесенная к 1 кг вещества с=С/m, Дж/кгК.
- молярная теплоемкость – теплоемкость, отнесенная к 1 молю вещества =С/n, Дж/мольК.
- объемная теплоемкость – теплоемкость, отнесенная к 1 м3 вещества С’=С/n, Дж/ м3К.
Теплоемкость – функция процесса и зависит от рода рабочего тела, характера процесса и параметров состояния. Так, теплоемкость в процессе с постоянным давлением называется изобарной теплоемкостью:
, (23)
где Н, Дж – энтальпия.
Теплоемкость в процессе с постоянным объемом называется изохорной теплоемкостью:
, (24)
где U, Дж – внутренняя энергия.
Уравнение Майера связывает между собой теплоемкости идеального газа в процессах p=const и v=const.
, (25)
где R – удельная газовая постоянная, зависящая от рода газа, или , Дж/кгК.
Отношение изобарной теплоемкости к изохорной теплоемкости называется показателем адиабатного процесса:
. (26)
Для реальных газов показатель k зависит от температуры. Для воздуха и двухатомных газов показатель температуры k=1.4.
Для смеси газов теплоемкость вычисляется как сумма теплоемкостей газов, входящих в состав смеси:
. (27)ние: