1)NaOH = Na⁺ + OH⁻
2)CuNO₃ = Cu²⁺ + NO₃²⁻
3)Na₂SO₄ = 2Na⁺ + SO₄²⁻
4)HCl = H⁺ + Cl⁻
5)H₂S = 2H⁺ + S²⁻
6)Na₃PO₄ = 3Na⁺ + PO₄³⁻
Задача №1
- Уравнение:
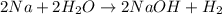
- вычислим количество вещества водорода:
n = V/Vm = 4,48л/22,4л/моль = 0,2 моль
- По уравнению реакции:
n(Na) = 2n(H2) = 0.2моль*2 = 0,4 моль
- Вычисляем массу натрия:
m(Na) = n*M = 0,4моль*23г/моль = 9,2 грамма
Отвеот: масса натрия равна 9,2 грамма
Задача №2
- Уравнение:
CuO + H2 = Cu + H2O
-По уравнению реакции, видим, что:
n(H2) = n(CuO) = 1,5 моль
- Масса 1,5 моль водорода:
m= n*M = 2г/моль*1,5моль = 3 грамма
- По уравнению реакции, видим, что:
n(Cu) = n(CuO) = 1.5 моль
- Рассчитывеам массу 1,5 моль меди:
m = n*M = 1,5 моль*64г/моль = 96 грамм
NaOH= Na(+) + OH(-)
CuNo3= Cu(2+) + 2NO3(-)
Na2SO4= 2NA(+) + SO4(2-)
HCl= H(+) + Cl(-)
H2S= H(+) + HS(-)
Na3PO4= 3Na(+) + PO4(3-)