Я так понимаю нужно сделать то, что обведено кружком.
Для того чтобы распознать в какой пробирке находится сульфат калия, а в какой карбонат калия нужно добавить соляную кислоту.
В пробирке с сульфатом калия никаких изменений не произойдет, т.к. данная соль с соляной кислотой не реагирует.
K2SO4 + HCl≠ (т.к. сульфат калия является солью сильной кислоты (серной), то реакция с другой сильной кислотой не происходит.)
В пробирке с карбонатом калия произойдет выделение углекислого газа.
K2CO3 + 2HCl (разб.) → 2KCl + CO2↑ + H2O
2K⁺ + CO²⁻3 + 2H⁺ + 2Cl⁻ → 2K⁺ +2Cl⁻ + CO2↑ + H2O
CO3²⁻ + 2H⁺ → CO2↑ + H2O
Для того чтобы распознать в какой пробирке находится сульфат натрия, а в какой силикат натрия нужно добавить соляную кислоту.
В пробирке сульфатом натрия никаких изменений не произойдет т.к. данная соль с соляной кислотой не реагирует.
Na2SO4 + HCl≠ (т.к. сульфат натрия является солью сильной кислоты (серной), то реакция с другой сильной кислотой не происходит.)
В пробирке с силикатом натрия выпадет белый студенистый осадок, т.к. это качественная реакция на силикат-ион, нерастворимые кремниевые кислоты осаждаются в виде осадка.
Na2SO4 + 2HCl (разб.) → 2NaCl + H2SiO3↓
2Na⁺ + SiO3²⁻ + 2H⁺ + 2Cl⁻ → 2Na⁺ + 2Cl⁻ + H2SiO3↓
2H⁺ + SiO3²⁻ → H2SiO3↓
Объяснение:
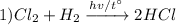
Реакция взаимодействия газообразных хлора и водорода на свету или при нагревании, с получением хлороводорода, реакция соединения
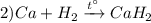
Реакция взаимодействия металлического кальция с парами водорода при нагревании, с образованием гидрида кальция, реакция соединения
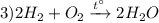
Реакция взаимодействия водорода с кислородом, с образованием воды, стехиометрическое количество смеси называется гремучий газ, реагирует с мгновенным взрывом и большим выделением тепла, реакция соединения
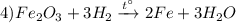
Взаимодействие оксида железа (III) с водородом при нагревании, с образованием железа и воды, возможен вариант взаимодействия с углем, алюминием или угарным газом, реакция замещения
Объяснение:
НСl - соляная к-та
С индикаторов: лакмус - красного цвета; метилоранж - розовый
HCl + AgNO₃ = AgCl↓ + HNO₃
H⁺ + Cl⁻ + Ag⁺ + NO₃⁻ = AgCl↓ + H⁺ + NO₃⁻
Ag⁺ + Cl⁻ = AgCl↓ выпадает осадок белого цвета
KOH - гидроксид калия - щелочь (основание, растворимое в воде)
индикаторов: лакмус - синего цвета; фенолфталеин - малинового цвета, метилоранж - желтого цвета.
AgNO₃ - нитрат серебра - соль
С реакции ионного обмена:
AgNO₃ + NaCl = AgCl↓ + NaNO₃
Ag⁺ + NO₃⁻ + Na⁺ + Cl⁻ = AgCl↓ + Na⁺ + NO₃⁻
Ag⁺ + Cl⁻ = AgCl↓ - осадок белого цвета
Na₂SO₃ можно определить, действуя на сульфит натрия сильной кислотой, выделяется газ с резким запахом:
Na₂SO₃ + 2HCl = 2NaCl + H₂O + SO₂↑
2Na⁺ + SO₃²⁻ + 2H⁺ + 2Cl⁻ = 2Na⁺ + 2Cl⁻ + H₂O + SO₂↑
2H⁺ + SO₃²⁻ = H₂O + SO₂↑