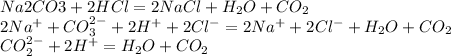1) Определяем массу серной кислоты, которая содержится в 400 г 9,8% раствора. В 100 г р-ра содержится 9,8 г H2SO4 а в 400 г р-ра Х г H2SO4 X = 400*9,8/100 = 39,2 г 2) Определяем молярные массы интересующих нас в-в: М (H2SO4) = 2*1 + 32 + 4*16 = 98 г/моль М (КОН) = 39 + 16 + 1 = 56 г/моль 3) Ур-ие реакции: 2КОН + H2SO4 = K2SO4 + 2H2O 4) Из ур-ия реакции видно, с 1 молем серной кислоты (98 г) реагируют 2 моля гидроксида калия (112 г) . На основании ур-ия составляем пропорцию: 98 г H2SO4 реагирует с 112 г КОН 39,2 г H2SO4 X г КОН Х = 39,2*112/98 = 44,8 г
1) Определяем массу серной кислоты, которая содержится в 400 г 9,8% раствора. В 100 г р-ра содержится 9,8 г H2SO4 а в 400 г р-ра Х г H2SO4 X = 400*9,8/100 = 39,2 г 2) Определяем молярные массы интересующих нас в-в: М (H2SO4) = 2*1 + 32 + 4*16 = 98 г/моль М (КОН) = 39 + 16 + 1 = 56 г/моль 3) Ур-ие реакции: 2КОН + H2SO4 = K2SO4 + 2H2O 4) Из ур-ия реакции видно, с 1 молем серной кислоты (98 г) реагируют 2 моля гидроксида калия (112 г) . На основании ур-ия составляем пропорцию: 98 г H2SO4 реагирует с 112 г КОН 39,2 г H2SO4 X г КОН Х = 39,2*112/98 = 44,8 г
а)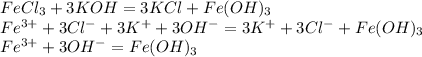
б)