Первой реакцией является реакция с хлоро-содержащим окислителем (реакция с HCl не подходит из-за слабой окислительной вместо Железа (3) получим Железо (2))
1) 2Fe+3Cl2=2FeCl3;
Поскольку гидроксид железа (3) - нерастворимое вещество, можно его получить реакцией со щелочью:
2) FeCl3+3NaOH=Fe(OH)3+3NaCL;
Разложение термически неустойчивого гидроксида приводит к оксиду железа (3):
3)2Fe(OH)3=Fe2O3+3H2O (разложение при температуре);
Восстановление оксида железа (3) водородом при повышенной температура даст желаемый продукт:
4) Fe2O3+3H2=2Fe+3H2O.
 моль ⇒ n(C)=0,3 моль
моль ⇒ n(C)=0,3 моль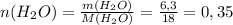 моль ⇒ n(H)=0,7 моль
моль ⇒ n(H)=0,7 моль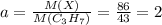
NH4Cl=NH3+HCl
m(NH4Cl)=175г
примеси-8%
M(NH4Cl)=14+4+35=53 г/моль
V(NH3)-?
175 г-100%
х г- 8%
х=8х175/100=14г-примеси
175-14=161 г чистый хлорид аммония
n(NH4Cl)=161/53=3 моль
n(NH4Cl)=n(NH3)=0.3моль по реакции
V(NH3)=n(NH3)хVm=3х22,4=67,2 л