Примеры участия металлов в реакции: а)соединения(три уравнения реакции) б)замещения(два уравнения реакции).составте схемы электронного и укажите,какова роль металлов в этих реакциях.
Дано: V( р-ра H2SO4) = 0,25 м3 w = 0,1 плотность(р-ра) = 1066 кг/м3 Найти: V (H2) Решение: Уравнение реакции: Сa + H2SO4 = CaSO4 +H2 m (р-ра H2SO4) = V(р-ра) * плотность = 0,25*1066= 266,5 кг m ( H2SO4) = m(р-ра) * w = 266,5* 0,1 = 26,65 кг n (H2SO4) = m/M = 26,65/98 = 0,27 примерно = 0,3 моль n(H2SO4) = n(H2) = 0,3 моль V(H2) = n * Vm = 0,3 * 22,4 = 6,72 л ответ: V( H2) = 6,72л Как-то так вроде, только я тогда не поняла смысл менять элеиенты( ну типо Са и т.д.), ответ то всё равно будет одинаковый, так что не знай правильно или нет
0 0 +2 -2
а)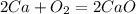
0 +2
Ca - 2e = Ca |2|восстановитель(окисление)
0 -2
O2 +4e = 2O |1|окислитель(восстановление)
0 +3 +3 0
б)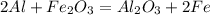
0 +3
Al - 3e = Al |2|восстановитель(окисление)
+3 0
2Fe + 6e =2Fe |1|окислитель(восстановление)
Металлы в таких случаях выступают как восстановители