a) Дано:
V(H2) = 1,2 л
V(Cl2) = 2,4 л
V(HCl) - ?
H2 + Cl2 = 2HCl
n(H2) = V(H2)/VA = 1,2 л / 22,4 л/моль = 0,05 моль
n(Cl2) = V(Cl2)/VA = 2,4 л / 22,4 л/моль = 0,1 моль
0,05 < 0,1
Cl2 в избытке, расчет по H2
n(HCl) = 2n(H2) = 2*0,05 = 0,1 моль
V(HCl) = n(HCl)*VA = 0,1 моль * 22,4 л/моль = 2,24 л
ответ: 2,24 л
б) Дано:
m(AgNO3) = 17 г
n(NaCl) = 0,2 моль
AgNO3 + NaCl = AgCl↓ + NaNO3
M(AgNO3) = 108 + 14 + 16*3 = 170 г/моль
n(AgNO3) = m(AgNO3)/M(AgNO3) = 17 г / 170 г/моль = 0,1 моль
0,1 < 0,2
NaCl - в избытке, расчет по AgNO3
n(AgNO3) = n(AgCl)
M(AgCl) = 108 + 35,5 = 143,5 г/моль
m(AgCl) = n(AgCl)*M(AgCl) = 0,1 моль * 143,5 г/моль = 14,35 г
ответ: 14,35 г
1. А) N2 + 3Н2 = 2NН3 - соединения
Б) 3Mg + 2H3РО4 = Mg3(РО4)2 +3 H2↑ - замещения
В) 2Al(OH)3 = Al2O3 + 3H2O - разложения
Г) 2Cu2O = 4Cu + O2↑ - разложения
2. Na2CO3 + 2HCl = 2NaCl + H2O + CO2 - ионного обмена.
признаки: выделение воды и газа, индикатор показывает нейтральный pH (в первом растворе (Na2CO3) изначально показывалась щелочная среда, во втором (HCl) - кислая)
2 + + 2+2=2+2+ H2O + CO2
+ 2=H2O + CO2
3. 2Mg+O2=2MgO
Магний+кислород=оксид магния
MgO+2HCl=MgCl2+H2O
оксид магния+соляная кислота=хлорид магния +вода
MgCl2+2KOH=Mg(OH)2+2KCl
хлорид магния+гидроксид калия= гидроксид магния + хлорид калия
4. 2 + 6 =2 +3
--3e-> 3 2 окислитель
2-+2e-> 2 3 восстановитель
Объяснение:
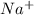

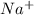
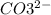

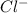


ответ:а) 3-метилпентен-2; б) бутен-1; в) 5-метин-4-этингексен-1
Объяснение: