1.Распределите вещества по классам, назовите вещества:
HCl, Na2O, KOH, H2SO4,HCl, CO2, Al2(SO4)3, HgO,SO2,Na3PO4
2.Даны вещества: оксид кальция, соляная кислота, оксид углерода (IV), вода, хлорид натрия. Какие из этих веществ будут взаимодействовать с гидроксидом бария? Напишите уравнения соответствующих реакций
3.Осуществите цепочку превращений:
S →SO2 → H2SO3
Na2SO3
4.Вычислите, какая масса хлора понадобится для окисления 7г железа.
 моль
моль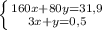
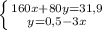

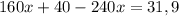

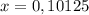 моль (это количество вещества Fe₂O₃)
моль (это количество вещества Fe₂O₃)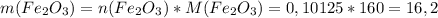 г
г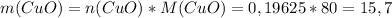 г
г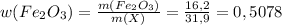 или 50,78% (где m(X) - это масса смеси)
или 50,78% (где m(X) - это масса смеси)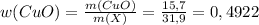 или 49,22%
или 49,22%
97.5g x
1.C6H6 + C3H6 = C6H5-C3H7
78g 120g
x=97.5·120/78=150g m=150·0.75=112.5g
112.5g x²
2.C6H5-C3H7 + O2 = C6H5-C3H7O2
120g 152g
x²=112.5·152/120=142.5 m=142.5·0.75=106.875g
106.875g x³
3.C6H5-C3H7O2 ⇒t⇒ C6H5-OH + C3H6O
152g 94g
x³=106.875·94/152=66g m=66·0.75=49.5g