Металлический алюминий получают электролизом раствора глинозема Al2O3 в расплавленном криолите Na2AlF6 при 960–970°С.
Процесс электролиза проводят в аппаратах, катодом в которых является подина ванны, а анодом – предварительно обожженные угольные блоки или самообжигающиеся электроды, погруженные в расплавленный электролит.
Электролиз Al2O3 можно представить следующей схемой:
в расплаве оксид алюминия диссоциирует:
Al2O3 = Al3+ + AlO33-,
на катоде восстанавливаются ионы Al3+:
Al3+ +3  Al0,
на аноде окисляются ионы AlO33-:
4AlO33- - 12  2Al2O3 + 3O2.
Суммарное уравнение процесса:
2Al2O3  4Al + 3O2.
Жидкий алюминий собирается на дне электролизера.
Алюминий высокой чистоты (не более 0,05 % примесей) получают электролитическим рафинированием чернового алюминия. Для получения алюминия особой чистоты (не более 0,001 % примесей) применяют зонную плавку или химическую транспортную реакцию:
2Al (ж) + AlF3 (г) = 3AlF (г).
1) литий - распределение электронов по уровням - 2, 1, неон - 2,8 - электроны расположены на двух энергетических уровнях - элементы второго периода
магний - 2,8,2 - электроны расположены на трех энергетических уровнях - элемент третьего периода
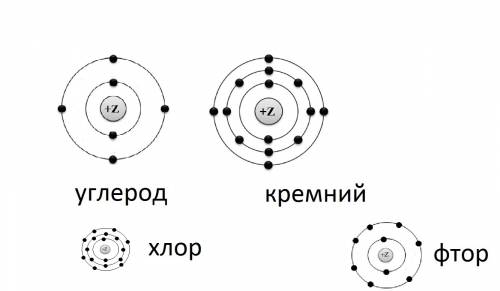
2) см. рисунок
3) а) у атомов кислорода и серы 6 электронов во внешнем слое. у атома кислорода 8 электронов расположены на двух энергетических уровнях,
у атома серы 16 электронов расположены на трех энергетических уровнях
б) у атомов серы и хлора электроны расположены на трех энергетических уровнях . у серы 6 электронов во внешнем слое, у хлора 7 электронов во внешнем слое
ответ:авд
Объяснение:коклп