20 г
Объяснение:
Напишем взаимодействие оксида серы с водой (в будущем это нам пригодится)
SO₃ + H₂O = H₂SO₄
Считаем массу начального раствора
m(раствора) = ρ * V(раствора) = 1.8 * 55.6 = 100 г
Считаем массу кислоты в нем
m(H₂SO₄) = w * m(раствора) = 0.91 * 100 = 91 г
Пусть количество вещества поглощенного оксида серы х моль. Тогда его масса 80х г. Масса образовавшейся кислоты 98х г. Такие выводы мы сделали из уравнения химической реакции Подставим все это в формулу
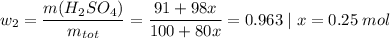
Ну и посчитаем массу оксида серы
m(SO₃) = M(SO₃) * n(SO₃) = 80 * 0.25 = 20 г
Объяснение:
8. Для окислительно-восстановительной реакции
Zn + Cu(NO3)2 = Cu + Zn(NO3)2
окислитель Cu(2+)
восстановитель Zn
процесс окисления Zn - 2e = Zn(2+)
процесс восстановления Cu(2+) + 2e = Cu(0)
9. Уравнение окислительно-восстановительной реакции
Fe2O3 + 3CO = 2Fe + 3CO2
Химическое количество восстановленного железа составляет 2,4 моль. Укажите:
массу восстановителя 100,80 г
объем углекислого газа (н.у.) 80,64 дм3
массу оксида железа (II) 192 г
объем оксида углерода (II) 80,64 дм3
Схема окислительно-восстановительной реакции:
Al + HCl > AlCl3 + H2↑
Масса алюминия вступившего в реакцию с соляной кислотой составляет 33,75 г. Укажите:
объем водорода (н.у.) 42 дм3
массу хлороводорода 136,88 г
массу водорода 3,75 г
массу соли 166,88 г
Задачи решены верно. Возможно в ответах опечатки
Объяснение:
2Mg(NO3)2 = 2MgO + 4NO2 + O2
2NO2 + H2O = HNO2 + HNO3
2HNO3 + Ca(OH)2 = Ca(NO3)2 + 2H2O