6 г х моль
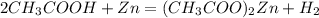
120 г 1 моль
1. Знайдемо чисту массу етанової кислоти у розчині:
m(CH3COOH)=m(розчину)*w(CH3COOH)=50*0,12=6 г
2. Підставивши цю масу у рівняння,розрахуємо кількість речовини водню:
при взаємодії 120 г кислоти виділяється 1 моль водню, а
при -- // -- 6 г____________________х г, звідки
х=6*1/120=0,05 моль
3. А тепер з формули по визначенню кількості речовини, знайдемо:
а) m(H2)=M(H2)*v(H2)=2*0,05=0,1 г
б) V(H2)=Vm(H2)*v(H2)=22,4*0,05=1,12 л
Объяснение:
1. Составим уравнение реакции:
2. Рассчитаем количество вещества прореагировавшего алюминия:
= 5,4 г : 27 = 0,2 моль.
3. Определим количество вещества, массу вступившей в реакцию кислоты и её массовую долю в исходном растворе:
= 0,6 моль;
= 0,6 моль · 36,5 г/моль = 21,9 г;
= 21,9 г : 219 г = 0,1 = 10%.