1. При прибавлении к раствору цитрата избытка известковой воды на холоду осадка не образуется. При нагревании же выпадает хлопьевидный осадок цитрата калия, при охлаждении (в закрытой колбе) вновь растворяющийся.
2. Нагревают 5 мл 1%-ного раствора лимонной кислоты с 1 мл реактива Дениже (5 г окиси ртути растворяют в смеси 20 мл концентрированной серной кислоты и 100 мл воды при нагревании до кипения) и прибавляют несколько капель 2%-ного раствора пер-манганата калия. Жидкость обесцвечивается и выпадает белый кристаллический осадок:
Промытый осадок растворяется в растворе хлорида натрия с образованием хлорида ртути и ацетон-дикарбоновой кислоты, которая с хлоридом железа дает малиново-красное окрашивание. 3. Реакция образования пентабромацетона
К водному раствору лимонной кислоты или цитрата в очень разбавленной серной или азотной кислоте (но не соляной) прибавляют
2-5 капель 0,1 н. раствора перманганата калия и нагревают в течение непродолжительного времени до 30-40° (только не кипятить!). Как только раствор побуреет или помутнеет от незначительного выделения двуокиси марганца, прибавляют 1-2 капли раствора ок-салата аммония и 1 мл 10%-ной серной кислоты, при этом жидкость становится прозрачной. Затем прибавляют несколько капель бромной воды. При этом выделяется кристаллический осадок пента-бромацетона.1
4.Глюкоза даёт синее окрашивание с свежеприготовленным Сu(OH)2. Даёт реакцию серебрянного зеркала с Ag(NH3)2OH/
Таким образом, если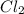 имеет степень окисления +7, в формуле мы его удваиваем (получается +14). Чтобы из 14 получить 0, необходимо отнять 14 (-14),
имеет степень окисления +7, в формуле мы его удваиваем (получается +14). Чтобы из 14 получить 0, необходимо отнять 14 (-14), 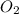 имеет степень окисления -2, значит, мы берём 7
имеет степень окисления -2, значит, мы берём 7 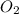 . В итоге получаем
. В итоге получаем 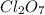 .
.
Для справки,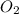 ,
, 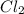 ,
, 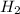 и ещё некоторые элементы пишутся с двойкой внизу, даже если они берутся в количестве одной единицы. K (Калий) в их число не относится, поэтому мы не пишем
и ещё некоторые элементы пишутся с двойкой внизу, даже если они берутся в количестве одной единицы. K (Калий) в их число не относится, поэтому мы не пишем 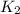 .
.