Метафосфорная кислота HPO3 взаимодействует с водой, растворяясь в ней:
HPO3 + H2O ® H3PO4
HPO3 H2O ® HPO3 + H2O ® H3PO3
Ни газ, ни осадок при этом не образуются, поэтому масса конечного раствора сложится из масс воды и метафосфорной кислоты:
m p-pa (H3PO4) = 100 г + 50 г = 150 г
Массу полученной ортофосфорной кислоты можно найти не только через моли, но и с пропорции:
100 г х г
HPO3 + H2O ® H3PO4
80 г 98 г
х = m (H3PO4) = 98 г · 100 г : 80 г = 122,5 г
w (H3PO4) = m (H3PO4) : m р-ра = 122,5 г : 150 г = 0,817 = 81,7%
При плавлении солей карбоновых кислот со щелочами образуются сответственные предельные углеводороды,поэтому выйдет такое уравнение:
4,8 г 3,6 г
40 г х г
1. Найдем молекулярную массу углеводорода:
при взаимодействии 4,8 г гидроксида образуется 3,6 г углеводорода, а
при --//--//-- 40 г___________________х г, откуда
х=40*3,6/4,8=30 г
2. Зная общую формулу предельных углеводородов и подставив эту массу(цифру) в формулу по вычислению относительной молекулярной массы,получим уравнение: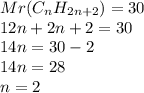 ,значит формула углеводорода:
,значит формула углеводорода: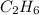 - это этан
- это этан