5 г х г
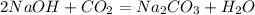
80 г 106 г
1. Сначала найдем чистую массу гидроксида в растворе(просто умножив массу раствора на массовую долю гидроксида в нем):
m(NaOH)=m(раствора)*w(NaOH)=20*0,25=5 г
2. Подставив эту массу в уравнение реакции,и получим массу соли(карбоната натрия):
при взаимодействии 80 г гидроксида получается 106 г карбоната, а
при --//--//-- 5 г_____________________х г, откуда
х=106*5/80=6,625 г
Газ - оксид углерода (IV) или углекислый газ
Объем - 11,2 л
Объяснение:
Пишем реакцию и сверху проставляем массы, а снизу молярную масса карбоната кальция и молярный объем газа:
50 x
CaCO₃ + 2HCl → CaCl₂ + CO₂↑ + H₂O
100 22,4
Составляем пропорцию и решаем ее крест-накрест:
50 --- x
100 --- 22,4
P.S.
• Почему под CaCO₃ 100? Это молярная масса, которая считается как сумма атомных масс элементов, входящих в вещество. Эти атомные массы можно взять в таблице Менделеева:
M(CaCO₃) = Ar(Ca) + Ar(C) + Ar(O)·3 = 40+12+16·3 = 100 г/моль
• Почему под CO₂ 22,4? Это молярный объем, который для всех газов при нормальных условиях равен 22,4 л/моль.