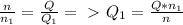
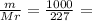 4,4 моль
4,4 моль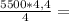 6,050 кДЖ
6,050 кДЖ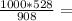 581,5г
581,5г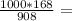 185г
185г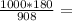 198,25г
198,25г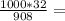 35,25г
35,25г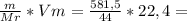 296л
296л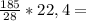 148л
148л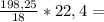 246,7л
246,7л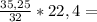 24,675л
24,675лТо есть концентрация полученного раствора должна стать: 15 + 5 = 20%
1) Если концентрацию раствора выразить в долях единицы, то массу растворенного вещества в граммах находят по формуле:
m(в-во) = ω * m(p-p)
где: m(p-p) - масса раствора в граммах, ω - массовая доля растворенного вещества, выраженная в долях единицы .
15% - это 0,15 в долях единицы, а 20% - 0,2
2) Обозначим массу раствора после упаривания через Х граммов. Так как при упаривании масса растворенного вещества не изменяется, то можем записать:
0,18 · 800 = 0,2 · Х
0,2Х = 120
Х = 600
3) То есть масса раствора была 800 г, а стала 200 г. Значит количество выпаренной воды равно:
800 - 600 = 200 г
ответ: 200 г воды
Объяснение:
) Ba(OH)2 + 2HCl = BaCl2 + 2H2O
Ba(OH)2 + N2O5 = Ba(NO3)2 + H2O
N2O5 + H2O = 2HNO3
18,5 г Х г
2) Ca(OH)2 + 2HNO3 = Ca(NO3)2 + 2H2O
n=1 моль n=2 моль
М=74 г/моль М = 63 г/моль
m=74 г m=126 г
18,5 г Ca(OH)2 - Х г HNO3
74 г Са(ОН)2 - 126 г HNO3
m(HNO3) = 18,5 * 126 / 74 =31,5 г