Дано:
t₁ = 150°C
t₂ = 200°C
Найти:
υ - ?
Правило Вант-Гоффа гласит, что увеличение (уменьшение) температуры на каждые 10°С приводит к увеличению (уменьшению) скорости реакции (зависит от коэффициента). Поскольку на каждые 10°С скорость увеличивается в 3 раза, математически это можно записать:
υ = υ₀ × γ^(t₂-t₁/10) - скорость реакции по прафилу Вант-Гоффа
υ = υ₀ × 3^(200°C - 150°C/10) = υ₀ × 3^(50/10) = υ₀ × 3⁵ = υ₀ × 234 = 243υ₀
Таким образом получаем, что скорость реакции увеличивается в 243 раза.
ответ: υ = 243υ₀ (в 243 раза)
Объяснение:
ZnCl2 + 2NaOH = Zn(OH)2↓ + 2NaCl
Zn(2+) + 2Cl(-) + 2Na(+) + 2OH(-) = Zn(OH)2↓ + 2Na(+) + 2Cl(-)
Zn(2+) + 2OH(-) = Zn(OH)2↓
Ba(NO3)2 + K2SO4 = BaSO4↓ + 2KNO3
Ba(2+) + 2NO3(-) + 2K(+) + SO4(2-) = BaSO4↓ + 2K(+) + 2NO3(-)
Ba(2+) + SO4(2-) = BaSO4↓
AlCl3 + 3KOH = Al(OH)3↓ + 3KCl
Al(3+) + 3Cl(-) + 3K(+) + 3OH(-) = Al(OH)3↓ + 3K(+) + 3Cl(-)
Al(3+) + 3OH(-) = Al(OH)3↓
FeCl2 + 2KOH = Fe(OH)2↓ + 2KCl
Fe(2+) + 2Cl(-) + 2K(+) + 2OH(-) = Fe(OH)2↓ + 2K(+) + 2Cl(-)
Fe(2+) + 2OH(-) = Fe(OH)2↓
Pb(NO3)2 + Na2SO4 = PbSO4↓ + 2NaNO3
Pb(2+) + 2NO3(-) + 2Na(+) + SO4(2-) = PbSO4↓ + 2Na(+) + 2NO3(-)
Pb(2+) + SO4(2-) = PbSO4↓
ZnCl2 + 2NaOH = Zn(OH)2↓ + 2NaCl
Zn(2+) + 2Cl(-) + 2Na(+) + 2OH(-) = Zn(OH)2↓ + 2Na(+) + 2Cl(-)
Zn(2+) + 2OH(-) = Zn(OH)2↓
Дано: розв'язання
m(AlCl3)=200г 200г х моль
m(осаду)=? AlCl3+3KOH=Al(OH)3+3KCl
v(осаду)=? 133,5г 1 моль
M(AlCl3)=133,5г Al(OH)3-осад
v (Al(OH)3 ) =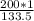 =1.5моль
=1.5моль
М(Al(OH)3 ) =78г
m=M*v
m(Al(OH)3 ) =78г*1,5=117г
Відповідь:маса=117г; кількість речовини =1,5моль
Объяснение: