Объяснение:
m(BaSO4) = 46,6 г
Объяснение:
Дано :
m(BaCl2) = 41.6 г
Найти :
m(BaS) - ?
BaCl2+Na2SO4 = BaSO4↓+2NaCl
В данной реакции осадком будет сульфат бария(BaSO4)
1) n(BaCl2) = m/M
M(BaCl2) = 137+35.5*2=208 г/моль
n(BaCl2) = 41,6 г/208 г/моль = 0,2 моль
n(BaCl2) = 0,2 моль
2) так как и у BaCl2 и у BaSO4 коэффиценты одинаковые =>
n(BaSO4) = n(BaCl2) = 0,2 моль
n(BaSO4) = 0,2 моль
3) m(BaSO4) = n*M
M(BaSO4) = 137+32+16*4 = 233 г/моль
m(BaSO4) = 0,2 моль * 233 г/моль = 46,6 г
m(BaSO4) = 46,6 г
ответ : m(BaSO4) = 46,6 г
х г 8,5 г у г
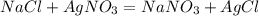
58,5 г 170 г 143,5 г
1. Сначала найдем массу нитрата серебра в растворе:
m(AgNO3)=m(раствора)*w(AgNO3)=170*0,05=8,5 г
2. Теперь,подставив эту массу в уравнение реакции,получим массу хлорида натрия:
для полного взаимодействия 58,5 г хлорида натрия необходимо 170 г нитрата,а
для -- // -- х г___________________________8,5 г, откуда
х=58,5*8,5/170=2,9 г
3. Так же через массу нитрата серебра,найдем массу осадка-хлорида серебра:
при взаимодействии 170 г нитрата выпадает 143,5 г хлорида, а
при -- // -- 8,5 г________________у г, откуда
у=8,5*143,5/170=7,2 г
Объяснение:
1)14-Si(кремний) период-3группа-4подгруппа-главнаяРяд-32)33-As(мышьяк)период-4группа-5подгруппа-главнаяРяд-53)48-Cd(Кадмий)период-5группа-2подгруппа-побочнаяРяд-7