общая формула альдегида CnH2nO
составим уравнение
(реакция сребрянного зеркала)
4.3 г 10.8г
CnH2nO + 2[Ag(nh3)2]OH= CnH2nO2 + 2Ag 3NH3 + h20
x 216
n(Ag)=2моль
M(ag)=108г/моль
m(ag)(по р-ции)=n*M=2*108=216г
m(CnH2nO)(по усл)=4.3г
найдем M(CnH2nO)
4.3/x=10.8/216
x=86
M(CnH2nO)=86г/моль
найдем какой же все таки альдегид, т.е. n
M(CnH2nO)=12n + 2n + 16 = 14n+16
14n+16=86
14n=70
n=5
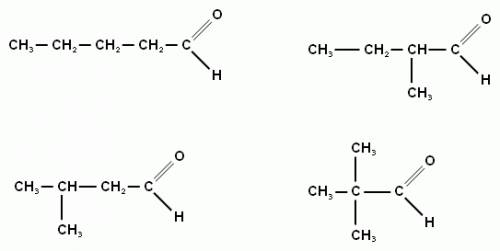
значит получится альдегид C5H10O или C4H9CHO
Пентаналь,2-метилбутаналь,3-метилбутаналь,2,2-диметилпропаналь
Известь кипелка - это СаО - негашёная известь!
1) Так как в известняке 6,7% примесей, то чистого известняка
(100 - 6,7) = 93,3%
А по массе это будет:
m(CaCO₃) = (22*93,3)/100 = 20,526 т = 20526 кг
2) Уравнение обжига известняка:
СаСО₃ → СаО + СО₂↑
3) Находим молярные массы:
М(СаО) = 40 + 16 = 56 г/моль = 0,056 кг/моль
М(СаСО₃) = 10 + 12 + 3*16 = 100 г/моль = 0,1 кг/моль
4) По уравнению реакции составляем пропорцию:
0,1 кг СаСО₃ 0,056 кг СаО
20526 кг СаСО₃ Х кг СаО
Х = 20526*0,056/0,1 = 11494,56 кг
ответ: 11494,56 кг СаО