1) Определите степень окисления химических элементов в приведенных веществах:
a) SO2
b) P2O3
c) Fe3O4
d) PH3
e) NH4Cl
f) Ba(NO3)2
g) K2Cr2O7
2) Подпишите степень окисления химических элементов, и определите какие реакции являются окислительно-восстановительными:
a) Fe + CuSO4= Fe SO4 +Cu
b) 2NO + O2 = 2 NO2
c) Fe(OH2) = FeO + H2O
d) Cu + Cl2= CuCl2
e) 2 NH3 + 3CuO =3Cu +N2 + H2O
f) 2NaNO3 = 2NaNO2 + O2
g) CuO + 2HCl = CuCl2 + H2O
3) Какой процесс окисления или восстановления отражает схема:
a) Al0 -3e -› Al+3
b) S0 +2e -› S-2
c) 2H+ +2e -› H20
d) Zn0 -2e -› Zn+2
4) Дополните фрагменты процессов окисления и восстановления, определите окислители и восстановители:
a) N0 -› N+2
b) P0 +2e -›
c) Cl-4 -› Cl0
d) Mn+4 ___-› Mn+2
e) ___ +2-› Cu0
5) Расставьте коэффициенты в следующих уравнениях химической реакции с метода электронного баланса, определите окислители и восстановители:
a) HCl +KMnO4 --› KCl +Mn Cl2 + Cl2 + H2O
b) Cu + HNO3 --› Cu(NO3)2 +NO + H2
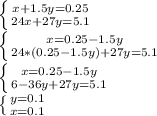 . Зная количество вещества каждого металла, можем найти массу этих металлов: m (Mg)=2.4 грамм, а m (Al)=2.7 грамм.
. Зная количество вещества каждого металла, можем найти массу этих металлов: m (Mg)=2.4 грамм, а m (Al)=2.7 грамм.
12. 2O(-2)-2e=O2 2 5 восстановитель
Mn(+7)+5e=Mn(+2) 5 2 окислитель
5H2O2+2K2MnO4+44H2SO4=5O2+2MnSO4+2K2SO4+4H2O
13. K2CO3+2HNO3=2KNO3+H2O+CO2
2H(+)+CO3(2-)=H2O+CO2
14.
540*0.6 x mol x L
6HCl + 2Al = 2 AlCl3 + 3H2
54g 2 mol 3*22.4 L
x mol=324*2/54=12 mol (AlCl3)
x L=324*3*22.4/54=403.2 L (H2)
15.
300*0.3=90g
150*0.25=37.5g
mrastvora2=300+150=450g
msoli2=90+37.5=127.5g
w2=127.5/450=0.283 или 28.3%