Что рекомендуется сделать с масляной краской (это суспензия твердых частиц красителя в жидкой основе) после длительного закачки перед ее использованием? Поясните свой ответ
4)А - я бы сказал не предыдущим, а последующим гомологом
5)А
6)В
7)А
8)Б
9)В
10)В
11) C₂H₅OH --H₂SO₄--> C₂H₄ + H₂O
C₂H₄ + HCl --> C₂H₅Cl
2C₂H₅Cl + 2Na --> C₄H₁₀ + 2NaCl
12) Формула C₅H₁₀
Межклассовая изомерия
CH₂=CH-CH₂-CH₂-CH₃ пентен-1
CH₃-CH=CH₂-CH₂-CH₃ пентен-2
Измерия углеродной цепи:
CH₂-CH-CH₃ метилциклобутан
| |
CH₂-CH₂
13) арены используются для производства ядов для насекомых и грызунов, их гомологи для производства красок смол , в качестве растворителей, в орг. синтезе
14)
Молярная масса углеводорода: M = D(H₂)*M(H₂) = 14*2=28 г/моль
На 100 г соединения приходится 85,7 г С и 14,3 г Н (в решении опечатка где-то - должно быть не более 100% суммарно).
Соотношение количеств элементов:
n(C) : n(H) = = 7,14 : 14,3 = 1:2
Формула CH₂
А так как молярная масса 28 г/моль, то C₂H₄, т.е. этен
ω(выхода Cu)-? 1. Определяем молярную массу оксида меди(ll): M(CuO)=64+16=80г./моль 2. Определяем количество вещества n в 40г. оксида меди(ll): n=m÷M n(CuO)=m(CuO)÷M(CuO)=40г.÷80г./моль=0,5моль 3. Запишем уравнение реакции восстановлении меди: CuO + CO= Cu + CO₂ 4. Анализируем уравнение реакции: по уравнению из 1 моль оксида меди(ll) образуется 1 моль меди, значит из 0,5 моль оксида меди(ll) образуется 0,5 моль меди 5. Определяем молярную массу меди: M(Cu)=64г./моль 6. Определяем массу меди количеством вещества 0,5 моль: m₂(Cu)= n(Cu)×M(Cu)= 0.5моль×64г./моль=32г. меди 7. Определяем массовую долю образования меди от теоретически возможного: ω(Cu)= m₁(Cu) ÷ m₂(Cu) =28г÷32г.=0,88 или ω%=ω(Cu)×100%=0,88×100%=88% 8. Массовая доля выхода меди от теоретически возможного составляет 0,88 или 88%
1)Б
2)В
3)А - не это не изомер, а это же вещество
4)А - я бы сказал не предыдущим, а последующим гомологом
5)А
6)В
7)А
8)Б
9)В
10)В
11) C₂H₅OH --H₂SO₄--> C₂H₄ + H₂O
C₂H₄ + HCl --> C₂H₅Cl
2C₂H₅Cl + 2Na --> C₄H₁₀ + 2NaCl
12) Формула C₅H₁₀
Межклассовая изомерия
CH₂=CH-CH₂-CH₂-CH₃ пентен-1
CH₃-CH=CH₂-CH₂-CH₃ пентен-2
Измерия углеродной цепи:
CH₂-CH-CH₃ метилциклобутан
| |
CH₂-CH₂
13) арены используются для производства ядов для насекомых и грызунов, их гомологи для производства красок смол , в качестве растворителей, в орг. синтезе
14)
Молярная масса углеводорода: M = D(H₂)*M(H₂) = 14*2=28 г/моль
На 100 г соединения приходится 85,7 г С и 14,3 г Н (в решении опечатка где-то - должно быть не более 100% суммарно).
Соотношение количеств элементов:
n(C) : n(H) =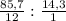 = 7,14 : 14,3 = 1:2
= 7,14 : 14,3 = 1:2
Формула CH₂
А так как молярная масса 28 г/моль, то C₂H₄, т.е. этен