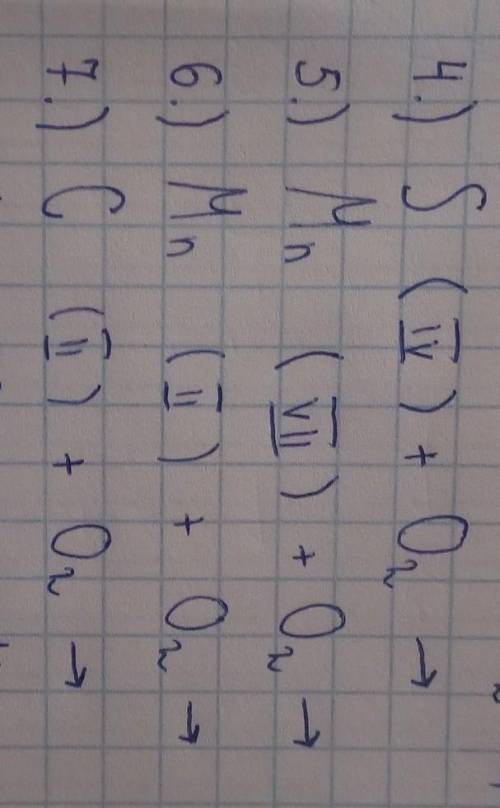
ответ:Комплексные щелочные цианидные электролиты отличаются простотой состава, наибольшей среди электролитов меднения рассеивающей и кроющей в них формируются мелкокристаллические, малопористые осадки.
Основой таких электролитов является комплексная цианистая соль меди и цианид калия или натрия. Другие компоненты вводят с целью повышения стабильности растворов и увеличения рабочего диапазона плотностей тока.
Медь находится в растворе в одновалентной форме и в присутствии даже небольшого количества свободного цианида образует соединение типа Na2[Cu(CN)3] или K2[Cu(CN)3]. Основным комплексным ионом, разряжающимся на катоде, является [Cu(CN)2]2-
[Cu(CN)2]2- + 2 → Cu + 2CN-. (12.г)
Процесс цианидного меднения идет с высокой катодной поляризацией, которая объясняется диффузионными ограничениями (концентрационное перенапряжение) и затруднениями разряда ионов. Катодное перенапряжение возрастает с повышением концентрации свободного цианида и уменьшением содержания меди в растворе. Это обстоятельство благоприятно сказывается на рассеивающей электролита, но одновременно приводит к снижению выхода металла по току и допустимой плотности тока. Как видно из рис. 12.1 для всех исследованных растворов наблюдается понижение выхода металла по току с увеличением плотности тока и в тем большей степени, чем меньше концентрация ионов меди и выше содержание свободного цианида. Эта закономерность повышению равномерности толщины покрытий на поверхности катода.
Объяснение:
- хімічні сполуки, що містять амонію іони. До А. с. належать гідроксид амонію і солі амонію (NH4C1, NH4NО3 тощо). Гідроксид амонію утворюється при розчиненні аміаку у воді, проявляє властивості слабкої основи внаслідок дисоціації. Більшість солей амонію розчинні у воді, дисоціюють у водних розчинах, гідролізуються. При нагріванні солі амонію розкладаються. Гідроліз і термічний розклад їх залежать від природи аніону. Напр., солі типу NH4C1, (NH4)2 SО4 розкладаються за схемою:
NH4C1 = NH3 + HCl. Якщо солі містять аніон-окислювач, при термічному розкладі відбувається окислювально-відновний процес:
NH4NО3 = N2О + 2N2О; (NH4)2 Cr2О7 = N2 + 4N2О + Cr2О3.
Солі амонію мають широке застосування. Так, хлорид амонію NH4C1 використовують у сухих батареях і як флюс для паяння та зварювання металів, а також як складову частину димоутворюючих сумішей. Сульфат (NH4)2SО4 і особливо нітрат NH4NО3
застосовують як азотні добрива; нітрат амонію в суміші з органічними речовинами та відновниками - як вибухові суміші. Гідрокарбонат амонію NH4HCО3 використовують у кондитерському виробництві.
S+O2=SO2
4Mn+7O2=2Mn2O7
2Mn+O2=2MnO
2C+O2=2CO