1)Первоначально ароматические углеводороды были названы так из-за характерного запаха. Сейчас ароматическими называют углеводороды, содержащие в молекуле одно или несколько бензольных колец. Общая формула ароматических углеводородов, в молекуле которых одно бензольное кольцо, CnH2n-6.
2)Представители ароматических углеводородов — бензол С6Н6 и его гомологи —имеют циклическое строение. Οʜᴎ могут иметь насыщенные или ненасыщенные боковые цепи. Некоторые из производных бензола обладают приятным запахом. По этой причине сохранилось их прежнее историческое название — ароматические углеводороды. Сегодня известны многие вещества, которые по строению и химическим свойствам следует отнести к ароматическим углеводородам. Бензол является самым типичным представителœем ароматических углеводородов, в молекуле которого шесть атомов углерода. Экспериментальные данные показывают, что в молекуле бензола 92,3 % углерода, как и в молекуле ацетилена. Следовательно, простейшая формула бензола должна быть такая же, как у ацетилена, — СН. Но плотность паров бензола по водороду равна 39, а масса его моля — 78 г (2DH = 2‣‣‣39). В случае если формула бензола действительно была бы СН, то масса его моля должна быть 13 г, а не 78 ᴦ. Следовательно, молекула бензола состоит из шести атомов углерода и шести атомов водорода (78 : 13 = 6), а его молекулярная формула С6Нб. Эксперименты показали, что при повышенной температуре и в присутствии катализаторов к каждой молекуле бензола присоединяются три молекулы водорода и образуется циклогексан. Этим доказывается, что бензол имеет циклическое строение. При этом эксперименты показали, что всœе связи в молекуле бензола равноценны. Согласно современным представлениям, в молекуле бензола у каждого атома углерода одно s- и два р-электронных облака гибридизованы (sp2-гибридизация), а одно р-электронное облако негибридизованное. Все три гибридизованных электронных облака, перекрываясь с гибридизованными облаками сосœедних атомов углерода и s-облаками атомов водорода, образуют три σ-связи, которые находятся в одной плоскости. Негибридизованные р-электронные облака атомов углерода расположены перпендикулярно плоскости направления σ -связей. Эти облака тоже перекрываются друг с другом (рис. 40). Рис. 40. Строение молекулы бензола В цикле молекулы бензола нет трех отдельных двойных связей: негибридизованное р-электронное облако первого атома углерода перекрывается с негибридизованными р-электронными облаками второго и шестого атомов углерода, а р-электронное облако второго атома углерода перекрывается с негибридизованными р-электронными облаками первого и третьего атомов углерода Так как электронная плотность в молекуле бензола распределœена равномерно, то правильнее структурную формулу бензола изображать в виде шестиугольника с окружностью внутри. Известно много сходных с бензолом ароматических углеводородов — гомологов бензола. Соединœения углерода и водорода, в молекулах которых имеется бензольное кольцо, или ядро, относятся кароматическим углеводородам. Сегодня используют формулу I (Фридриха Кекуле (1829-1896) 1865 ᴦ.) или III. Радикал –С6Н5 принято называть фенилом.
3)на картинке вроде как
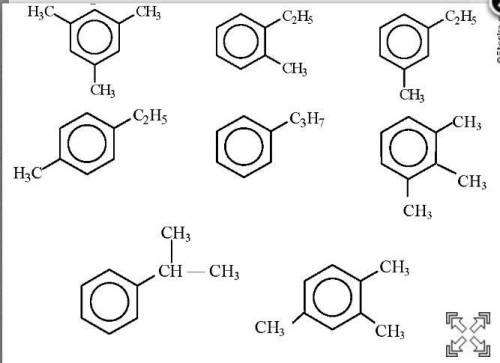
Объяснение:
1) К2О. оксид калия
ZnO. оксид цинка
Al2O3. оксид алюминия
CaCl2. хлорид кальция
NaH. гидрид натрия
HBr. бромоводород
2)Zn+2HBr=ZnBr2+H2
3H2+Cr2O3=2Cr+3H2O
H2+2K=2KH
3) 2Mg+O2=2MgO
C+O2=CO2
H2+Cl2=2HCl
4) 16 г. Х г
2H2. +. O2. =. 2H2O
n=2 моль. n=2 моль
М=2г/моль. М=18 г/моль
m=4 г. m=36 г
16 г. Н2. -. Х г. Н2О
4. г. Н2. -. 36 г. Н2О
m(H2O)=16*36/4=144 г
5). m(р-ра)=m(в-ва)+m(р-ля)=10+150=160 г
W(в-ва)=m(в-ва)/m(р-ра) *100%=10/160. *100%=6,25%
6) Na2O+H2O=2NaOH. соединение
2HgO=2Hg+O2. разложение
LiOH+HNO3=LiNO3+H2O. обмен
Mg+2HCl=MgCl2+H2. замещение
2H3PO4+3CaCl2=6HCl+Ca3(PO4)2
6H(1+)+2PO4(3-)+3Ca(2+)+6Cl(1-)=6H(1+)+6Cl(1-)+3Ca(2+)+2PO4(3-)