Кислота средней силы:
{\displaystyle ~{\mathsf {H_{2}SO_{3}\rightleftarrows H^{+}+HSO_{3}^{-{\displaystyle ~{\mathsf {HSO_{3}^{-}\rightleftarrows H^{+}+SO_{3}^{2-Существует лишь в разбавленных водных растворах (в свободном состоянии не выделена):
{\displaystyle ~{\mathsf {SO_{2}+H_{2}O\rightleftarrows H_{2}SO_{3}\rightleftarrows H^{+}+HSO_{3}^{-}\rightleftarrows 2H^{+}+SO_{3}^{2-Растворы H2SO3 всегда имеют резкий специфический запах химически не связанного водой SO2.
Двухосновная кислота, образует два ряда солей: кислые — гидросульфиты (в недостатке щёлочи):
{\displaystyle {\mathsf {H_{2}SO_{3}+NaOH\longrightarrow NaHSO_{3}+H_{2}O}}}и средние — сульфиты (в избытке щёлочи):
{\displaystyle {\mathsf {H_{2}SO_{3}+2NaOH\longrightarrow Na_{2}SO_{3}+2H_{2}O}}}Как и сернистый газ, сернистая кислота и её соли являются сильными восстановителями:
{\displaystyle {\mathsf {H_{2}SO_{3}+Br_{2}+H_{2}O\longrightarrow H_{2}SO_{4}+2HBr}}}При взаимодействии с ещё более сильными восстановителями может играть роль окислителя:
{\displaystyle {\mathsf {H_{2}SO_{3}+2H_{2}S\longrightarrow 3S\downarrow +3H_{2}O}}}Качественная реакция на сульфит-ионы — обесцвечивание раствора перманганата калия:
{\displaystyle {\mathsf {5SO_{3}^{2-}+6H^{+}+2MnO_{4}^{-}\longrightarrow 5SO_{4}^{2-}+2Mn^{2+}+3H_{2}O}}}
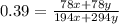
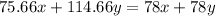
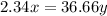
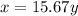
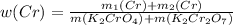
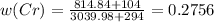 или 27.56%
или 27.56%
Объяснение:
При сгорании в кислороде 4 г водорода выделяется 584 кДж теплоты. Какую массу водорода нужно сжечь, чтобы выделилось 2920 кДж?
2 моль
2Н2 + О2 = 2Н2О + 584 кДж
При сгорании 2 моль водорода выделяется 584 кДж
2950 кДж : 584 кДж = 5,05 х 4 = 20,2 г водорода.
В растворе хлорида натрия с массовой долей солей равной 10% растворили еще 20 г той же соли. Какой стала массовая доля соли в полученном растворе, если масса исходного раствора равна 180 г?
Масса исходного раствора 180 г. Вычислим массу растворенного вещества в этом растворе: 180 × 0,1 = 18 г
Добавляя в раствор определенную массу соли мы увеличиваем и массу растворенного вещества и массу раствора:
18 +20 38
ω = = ×100 = 19%
180 +20 200
Напишите уравнения диссоциации серной кислоты, гидроксида натрия, нитрата алюминия, хлорида бария, соляной кислоты.
Н₂SO₄ ⇄ 2H⁺ + SO₄²⁻
NaOH ⇄ Na⁺ + OH⁻
Al(NO₃)₃ ⇄ Al³⁺ + 3NO₃⁻
BaCl₂ ⇄⇄ Ba²⁺ + 2Cl⁻
HCl ⇄ H⁺ + Cl⁻