Na₂CO₃ + SiO₂ = Na₂SiO₃ + CO₂
n(Na₂CO₃) = n(SiO₂) = n(Na₂SiO₃)
CaCO₃ + SiO₂ = CaSiO₃ + CO₂
n(CaCO₃) = n(SiO₂) = n(CaSiO₃)
Na₂SiO₃ + СaSiO₃ + 4SiO₂ = Na₂O*CaO*6SiO₂
M(Na₂O*CaO*6SiO₂) = 23*2+ 16 + 40+16 + 6*(28 + 2*16) = 478 г/моль
n= m/M = 100кг/478 кг/моль = 0,2092 кмоль, тогда
n(Na₂CO₃) = 0,2092 кмоль,
n(CaCO₃) = 0,2092 кмоль,
n(SiO₂) = 6*0,2092 кмоль, =1,2552 кмоль
m(Na₂CO₃) = n*M =0,2092 кмоль * 106 кг/моль = 22,175 кг
m(CaCO₃) = n*M =0,2092 кмоль * 100кг/моль = 20.92 кг
m(SiO₂) = n*M = 1,2552 кмоль * 60кг/моль = 75,31 кг
Na2CO3 + SiO2 = Na2SiO3 + CO2
n (Na2CO3) = n (SiO2) = n (Na2SiO3)
CaCO3 + SiO2 = CaSiO3 + CO2
n (CaCO3) = n (SiO2) = n (CaSiO3)
Na2SiO3 + СaSiO3 + 4SiO2 = Na2O*CaO*6SiO2
M (Na 2O*CaO*6SiO2) = 23*2 + 16 + 40+16 + 6 * (28 + 2*16) = 478 г/моль
n = m/M = 100 кг/478 кг/моль = 0,2092 кмоль, тогда
n (Na2CO3) = 0,2092 кмоль,
n (CaCO3) = 0,2092 кмоль,
n (SiO2) = 6*0,2092 кмоль, = 1,2552 кмоль
m (Na2CO3) = n*M = 0,2092 кмоль * 106 кг/моль = 22,175 кг
m (CaCO3) = n*M = 0,2092 кмоль * 100 кг/моль = 20.92 кг
m (SiO2) = n*M = 1,2552 кмоль * 60 кг/моль = 75,31 кг.
Все!( думаю так)
Составим уравнение и подпишем под ним то, что дано:
С₂Н₅ОН + Na => C₂H₅ONa + H₂↑
69 г х г
m (Na) = M×n
m (Na) = 22,98 г\моль 1 моль= 22,98 грамм.
m (H₂) = M×n
m (H₂) = 1 г\моль ×2 моль= 2 грамма
Составляем пропорцию:
69 г (Na) - х г (H₂)
22,98 г (Na) - 2 г (H₂)
Отсюда =>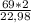 = 6,005 грамм.
= 6,005 грамм.
ответ: 6,005 грамм
Объяснение:
Т.к в уравнении мы имеем один Na, и зная его молярную массу из таблицы Менделеева 22,98 г\моль, то можем найти его массу:
m (Na) = M×n
m (Na) = 22,98 г\моль 1 моль= 22,98 грамм.
Аналогично находим массу водорода
В уравнении у нас H₂, значит количество водорода n=2 моль, молярная масса M(H) = 1 г\моль
m (H₂) = M×n
m (H₂) = 1 г\моль ×2 моль= 2 грамма