структурная изомерия - это когда меняется положение составляющих органического в-ва.
Например, бутан-н.
Н3С-Н2С-Н2С-СН3
и 2-метилпропан
H3С-HС-СH3
|
CH3
это структурные изомеры.
Пространственная изомерия - это когда составляющие орг. в-ва находятся в различных пространствах.
Допустим 1,2-диметил,3,4-дихлорциклобутан
СН3:::СH-СH:::Сl
| |
CH3-HC- CH-Cl
В данном в-ве 1 радикал метил и 1 хлор находятся над плоскостью, а 2 метил и 2 хлор под плоскостью.
СН3-СH-СH-Сl
| |
CH3:::HC- CH:::Cl
А в этом в-ве уже другие метил и хлор находятся над плоскостью(отмечено точками),а оставшиеся метил и хлор под плоскостью.
Эти два в-ва и будут пространственными изомерами.
1)изомер
2)изомер
3)изомер
4)гомолог
5)изомер
6)гомолог
1. А) N2 + 3Н2 = 2NН3 - соединения
Б) 3Mg + 2H3РО4 = Mg3(РО4)2 +3 H2↑ - замещения
В) 2Al(OH)3 = Al2O3 + 3H2O - разложения
Г) 2Cu2O = 4Cu + O2↑ - разложения
2. Na2CO3 + 2HCl = 2NaCl + H2O + CO2 - ионного обмена.
признаки: выделение воды и газа, индикатор показывает нейтральный pH (в первом растворе (Na2CO3) изначально показывалась щелочная среда, во втором (HCl) - кислая)
2 + + 2+2=2+2+ H2O + CO2
+ 2=H2O + CO2
3. 2Mg+O2=2MgO
Магний+кислород=оксид магния
MgO+2HCl=MgCl2+H2O
оксид магния+соляная кислота=хлорид магния +вода
MgCl2+2KOH=Mg(OH)2+2KCl
хлорид магния+гидроксид калия= гидроксид магния + хлорид калия
4. 2 + 6 =2 +3
--3e-> 3 2 окислитель
2-+2e-> 2 3 восстановитель
Объяснение:
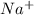

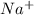
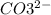

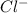


Объяснение:
1. К сожалению, это для вас задание ясно. Я вижу только не которые цифры. Но как я понял нужно приготовить 6% раствор сульфата магния, если имеется гептагидрат сульфата магния
MgSO4 ·7H2О.
Необходимо знать плотность плотность 6% раствора сульфата магния. Она в задании есть 1060,2 г/дм³ или 1,0602 г/см³
1. Рассчитаем массу 6% раствора MgSO4:
500 мл ≈ 500 см³ = 500 cм³ = 0,5 дм³
m (p-pa MgSO4 6%) = 0,5 дм³ × 1060.2г/дм3 = 530,1 г
2. Рассчитаем массу сульфата магния в этом растворе
m ( MgSO4) = 530,1 г × 0,06 = 31,8 г
3. Вычислим количество вещества безводного сульфата магния, которое соответствует массе 31,8 г
31,8 г : 120 г/моль = 0,265 моль.
Следовательно, что и в 0,265 моль MgSO4 ·7H2О будет содержаться такая же масса (31,8 г) безводного MgSO4.
4. Находим массу 0,265 моль кристаллогидрата MgSO4 ·7H2О:
246 г/ моль × 0,265 моль = 65,2 г
В этой навеске 65,2 г будет содержаться 31,8 г безводного сульфата магния и кристаллизационная вода 65,2 - 31,8 = 33,4 г.
Для приготовления 6% раствора сульфата магния отвешиваем на технохимических весах 65,2 г кристаллогидрата MgSO4 ·7H2О. Помещаем в колбу нужного объема (не обязательно мерную ведь мы готовим не раствор для титрования а обычный раствор с массовой долей 6%)
5. Рассчитаем теперь какую массу воды надо прилить.
По расчету масса раствора 530, 1, но часть воды уже находится в навеске кристаллогидрата.
m(H2O) = 530,1 - 65,2 = 464,9 см³ или округленно 465 мл.