кроме инертных газов неона и аргона , другие атомы химических элементов могут превращаться себя ионам. все атомы могут прикрепляв или потеряв электроны станут ионами. например: серебро на нитрате серебра или хлорида серебра
Объяснение:
инертные гази только они одноатомные гази. К инертным ным газам относятся гелий (He), неон (Ne), аргон (Ar), криптон (Kr), ксенон (Xe) и радиоактивный радон (Rn). Характеристики инертных газов объяснены современными теориями структуры атома: их электронные оболочки из валентных электронов являются заполненными, тем самым позволяя участвовать лишь в очень малом количестве химических реакций: известны всего несколько сотен химических соединений этих элементов. Наиболее «инертны» неон и гелий: чтобы заставить их вступить в реакцию,
с методов оптической спектроскопии и масс-спектрометрии установлено существование ионов Ne+, (NeAr)+, (NeH)+, и (HeNe)+.
1. Химические формулы веществ с ионной и ковалентной неполярной связью соответственно: 5)Li3S и K2O
2. Водородная связь образуется между молекулами: 3)Метанола 3. Длина связи водород-галоген изменяется в молекуле 4)HF 4. Электроотрицательность убывает в ряду химических элементов: 1)As, P, N; 5. Гомологами являются: 3)Бензол и гексан 6. Соединение, в котором одна из ковалентных связей образована по донорно-акцепторному механизму: 4)C2H5NH3OH; 7. Тип кристаллической решетки вещества, для которого характерны следующие свойства: низкая температура плавления, малая твердость и летучесть: 4)Ионная 8. Тип кристаллической решетки соединения, образованного химическими элементами с зарядами ядер атомов +16 и +19: 1)Ионная 9. Пентен-2 и циклопентан являются: 3)геометрическими изомерами 10. Пара элементов, каждая из которых имеет аллотропные видоизменения 2)S и O; 3)P и H;
кроме инертных газов неона и аргона , другие атомы химических элементов могут превращаться себя ионам. все атомы могут прикрепляв или потеряв электроны станут ионами. например: серебро на нитрате серебра или хлорида серебра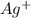
Объяснение:
инертные гази только они одноатомные гази. К инертным ным газам относятся гелий (He), неон (Ne), аргон (Ar), криптон (Kr), ксенон (Xe) и радиоактивный радон (Rn). Характеристики инертных газов объяснены современными теориями структуры атома: их электронные оболочки из валентных электронов являются заполненными, тем самым позволяя участвовать лишь в очень малом количестве химических реакций: известны всего несколько сотен химических соединений этих элементов. Наиболее «инертны» неон и гелий: чтобы заставить их вступить в реакцию,
с методов оптической спектроскопии и масс-спектрометрии установлено существование ионов Ne+, (NeAr)+, (NeH)+, и (HeNe)+.