ответ: дано: этилен-С2Н4
этан-С2Н6
масса продукта:6г
найти: объём этилена?
4,48л
Объяснение: решения :
С2Н4+Н2=С2Н6
22,4л Mr(C2H6)=12*2+1*6=24+6=30
22.4л-----30г
х л---------6
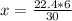
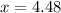 л
л
Теллуровая кислота — слабая многоосновная неорганическая кислота состава H6TeO6 (H2TeO4•2H2O), соответствующая высшей степени окисления теллура (+6)
Физические свойства
Бесцветные кристаллы, растворимые в воде, не растворяются в концентрированной азотной кислоте.
Получают взаимодействием элементарного теллура с 30%-м раствором перекиси водорода при нагревании на водяной бане. При температуре ниже 10 °С выделяется из раствора в виде кристаллогидрата H6TeO6•4H2O. Соли теллуровой кислоты могут быть получены растворением оксида теллура(VI) в концентрированных растворах щелочей либо сплавлением теллуритов с КNО3
Химические свойства
Слабая кислота; К1 = 2•10−8, К2 = 1•10−11. Относительно неустойчива; при нагревании до 140 °С образует аллотеллуровую кислоту — вязкую хорошо смешивающуюся с водой жидкость, представляющую собой, по-видимому, раствор смеси полимерных теллуровых кислот. Выше 300 °С распадается на TeO3 и воду.
Соли теллуровой кислоты — теллураты. На металл могут замещаться все атомы водорода, поэтому известны как частично (Na2H4TeO6), так и полностью замещённые (Na6TeO6) производные. Na6TeO6, получаемый сплавлением теллуровой кислоты с NaOH, на воздухе постепенно переходит в Na2H4TeO6•3H2O.
Молярная масса: 229,64 г/моль
Х л 6 г
СH2=CH2 + H2 -> CH3-CH3
n=1 моль n=1 моль
Vm=22,4 л/моль M = 30 г/моль
V = 22,4 л m=30 г
Х л С2Н4 — 6 г С2Н6
22,4 л С2Н4 — 30 г С2Н6
V(C2H4) = 22,4 * 6 / 30 = 4,48 л