В молекуле озона - три атома, кислорода - два атома. 3,6*10^20 против 2,4*10^13. Очевидно, в данной порции озона атомов больше, чем в данной порции кислорода.
Я не применял формулу = ; поскольку не указаны условия, а известное в пособиях значение константы Vm применяем для нормальных условий.
Формула алкадиенов СnH2n-2 M(HCl) = 36.5 г/моль M(СnH2n-2) = 12n+(2n-2) = 14n-2 г/моль Пусть масса алкадиена х г. Тогда масса хлороводорода 1,074х г. Уравнение реакции гидрогалогенирования (оно идет по обеим двойным связям, потому что по условию получается дигалогеналкан):
СnH2n-2 + 2 HCl = СnH2nCl2 х г 1,074х г (14n-2) г 2*36,5 г
Возможные варианты: изолированный, кумулированный, сопряженный диен. 1. Случай изолированного диена невозможен - в молекуле нет третичных атомов, соответственно, не может быть третичных галогенпроизводных:
H2C = CH - CH2 - CH = CH2
2. Случай кумулированного диена с третичным атомом углерода (выделен жирным шрифтом) возможен:
Br Br | | H3C - C = С = CH2 + Br2 ⇒ H3C - C - C = CH2 | | CH3 CH3
Однако полученное вещество является продуктом не 1,2-, а 2,3-присоединения.
3. Случай сопряженного диена с третичным атомом углерода возможен:
В порции озона. 3,6*10^20 против 2,4*10^13.
Объяснение:
Итак, основная формула - применяемая в этой задаче
N =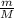 *Na, Na - число Авогадро, равное 6,022*10^23 моль⁻1, а N - число молекул
*Na, Na - число Авогадро, равное 6,022*10^23 моль⁻1, а N - число молекул
Для озона все проще - 0,0096 г/46 г/моль * 6,022*10^23 моль⁻1, ≈ 1,2044*10^20
Для кислорода все на шаг дольше, поскольку дан объем, а не масса. Эти две величины связаны соотношением V =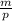 , отсюда m = V*p
, отсюда m = V*p
N =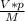 *Na = (0,00000448 м^3* 0,00143 г/м^3) * 6,022*10^23 моль⁻1, /32 г/моль ≈ 1,2056*10^13
*Na = (0,00000448 м^3* 0,00143 г/м^3) * 6,022*10^23 моль⁻1, /32 г/моль ≈ 1,2056*10^13
В молекуле озона - три атома, кислорода - два атома. 3,6*10^20 против 2,4*10^13. Очевидно, в данной порции озона атомов больше, чем в данной порции кислорода.
Я не применял формулу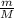 =
= 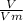 ; поскольку не указаны условия, а известное в пособиях значение константы Vm применяем для нормальных условий.
; поскольку не указаны условия, а известное в пособиях значение константы Vm применяем для нормальных условий.