4)Електролітична дисоціація - це процес розпаду молекул на іони при його розчиненні або плавлення.
3)Неелектролітів - речовини, розчини яких не проводять електричний струм. 5. До неелектролітів відносять прості речовини (метали і неметали), оксиди, більшість органічних речовин: вуглеводні, спирти, альдегіди, вуглеводи, прості і складні ефіри та ін.
2)Електроліти і неелектролітів
Електроліти - це речовини, розчини або розплави яких проводять електричний струм.
До електролітів належать лугу, розчинні солі і кислоти.
У водних розчинах електроліти розпадаються на іони.
1)Розчин цукру не є електролітом. Молекули цукру мають ковалентний неполярну зв'язок, при розчиненні цукру у воді руйнування його молекули і утворення заряджених іонів не відбувається, тому такий розчин електричного струму не проводить.
1. Сначала найдем относительную молекулярную массу оксида:
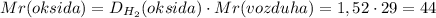
2. Теперь допустим,что валентность элемента в оксиде равно I, тогда формула оксида - 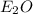 , подставив в формулу по вычислению молекулярной массы,получим уравнение:
, подставив в формулу по вычислению молекулярной массы,получим уравнение:
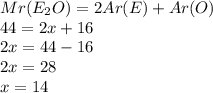
Химический элемент с относительной атомной массой 14 - это Азот, значит формула оксида: 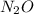 , т.е. оксид азота(I) или так называемый "веселильный газ",который долгое время использовали как анастезирующее
, т.е. оксид азота(I) или так называемый "веселильный газ",который долгое время использовали как анастезирующее
3. Теперь допустим,что элемент 4-х валентный,тогда формула оксида - 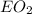 ?получим уравнение:
?получим уравнение:
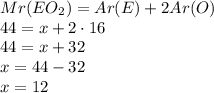
Химический элемент с относительной атомной массой 12 - Углерод,а формула оксида - 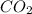 , т.е. оксид углерода(IV) или углекислый газ
, т.е. оксид углерода(IV) или углекислый газ
Если: а) в атоме элемента имеется 3 электронных слоя и на внешнем слое имеется пять электронов, то этот элемент расположен в 3 периоде в VА группе. Это неметалл фосфор.
б) у атома элемента имеется 13 протонов, значит его порядковый номер = 13. Это металл алюминий.
Фосфор и алюминий могут реагировать между собой с образованием фосфида алюминия:
Al + P → AlP (реакция идет при температуре 500°C)
Химическая связь в соединении фосфид алюминия ионная. Алюминий имеет 3 валентных электрона, которые отдает в процессе образования химической связи и превращается в положительный ион - катион Al⁺³.
Фосфор имеет 5 валентных электронов, ему не хватает трех электронов до завершения внешнего электронного уровня. Фосфор принимает 3 электрона и превращается в ион - анион P⁻³.
Между положительным и отрицательным ионами за счет электростатического притяжения образуется ионная связь.
Схема в приложении.