В общем, дам обычные ответы, которые бывают на к/р:
Кислород - типичный неметалл, газ, Ar(O)= 16г/моль; M(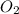 )= 32г/моль; В таблице Менделеева расположен в VI группе, главной подгруппе (подгруппа халькогены). Является сильным окислителем, проявляет св-ва восстановителя в соединениях с фтором.
)= 32г/моль; В таблице Менделеева расположен в VI группе, главной подгруппе (подгруппа халькогены). Является сильным окислителем, проявляет св-ва восстановителя в соединениях с фтором.
Подгруппа кислорода: Кислород, Сера, Селен, Теллур, Полоний. На внешнем уровне находится 6 электронов (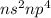 ), следовательно, максимальная валентность VI (Но! Исключение составляют кислород и фтор!). Валентности II, IV, VI свойственны сере, селену, теллуру и полонию, они проявляют степени окисления: -2, +2, +4 и +6. В соединениях с водородом и металлами проявляют степень окисления: -2, а в соединениях с кислородом и активными неметаллами: +4 и +6.
), следовательно, максимальная валентность VI (Но! Исключение составляют кислород и фтор!). Валентности II, IV, VI свойственны сере, селену, теллуру и полонию, они проявляют степени окисления: -2, +2, +4 и +6. В соединениях с водородом и металлами проявляют степень окисления: -2, а в соединениях с кислородом и активными неметаллами: +4 и +6.
Изменение св-в веществ: с увеличением заряда ядра радиус увеличивается, ослабевают неметаллические и возрастают металлические свойства.
Вроде бы, Всё!
-------------------------------------------------------------------------------------------------
Есть вопросы? Задавай Если человек знает, чего он хочет, значит, он или много знает, или мало хочет."
BaCO3+2HCl=BaCl2+H2O+CO2
Na2CO3+2HCl=2NaCl+H2O+CO2
BaCl2+Na2SO4=BaSO4(осадок)+2NaCl
в осадок в результате обработки избытком сульфата натрия выпадает сульфат бария (идет только реакция с хлоридом бария, реакция с хлоридом натрия не идет)...
количество вещества сульфата бария, выпавшего в осадок: m(BaSO4)/M(BaSO4)=(46.6г)/(233г/моль)=0,2 моль
карбоната бария было также 0,2 моль...
зная количество вещества и молярную массу карбоната бария (197 г/моль), находим массу карбоната бария: 0,2*197=39,4 г.
теперь находим долю карбоната бария в его смеси с карбонатом натрия:
m(BaCO3)*100%/(m(BaCO3)+m(Na2CO3))=39.4*100/50=78.8%
CH⁴=C+2H²
2.5моль. - Х литров H²
1моль. - 2× 22.4л
х=112литроа Н²