Объяснение:2 вопрос
алкан-сн4
алкен-с2н4
алкин-с2н2
3вопрос
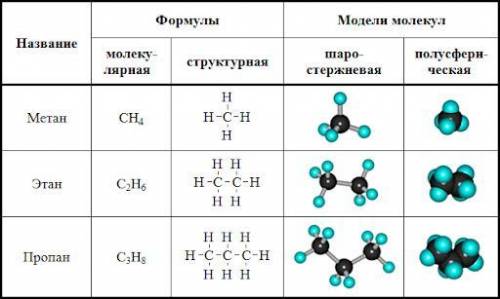
внизу будет картинка
4 вопрос
алкены:Температуры плавления и кипения алкенов (упрощённо) увеличиваются с молекулярной массой и длиной главной углеродной цепи.
При нормальных условиях алкены с C2H4 до C4H8 — газы; с пентена C5H10 до гептадецена C17H34 включительно — жидкости, а начиная с октадецена C18H36 — твёрдые вещества. Алкены не растворяются в воде, но хорошо растворяются в органических растворителях.
Алкины по своим физическим свойствам напоминают соответствующие алкены. Низшие (до С4) — газы без цвета и запаха, имеющие более высокие температуры кипения, чем аналоги в алкенах.
алкин: Алкины плохо растворимы в воде, лучше — в органических
растворителях.
5 вопрос
Реакция горения.
Все алканы горят. При этом образуются углекислый газ и вода и выделяется большое количество тепла:
Реакции замещения.
Алканы реагируют при освещении с галогенами (хлором и бромом). При этом постепенно происходит замещение атомов водорода в молекуле алкана на атомы галогена:
Реакции разложения.
При сильном нагревании алканы разлагаются на уголь и водород:
алкен: картинка ниже
алкин :картинка ниже


S
SO2
H2S
SO3
Объяснение: