Объяснение:
а) H₂O₂⁻¹+PbS⁻²→PbS⁺⁶O₄+H₂O⁻²
O⁻¹ +1e⁻→O⁻² 1 8
8
S⁻²-8e⁻→S⁺⁶ 8 1
O⁻¹ окислитель
S⁻² восстановитель
4H₂O₂+PbS=PbSO₄+4H₂O
б) CI⁺⁴O₂+NaOH→NaCI⁺³O₂+NaCI⁺⁵O₃+H₂O
CI⁺⁴+1e⁻→CI⁺³ 1
CI⁺⁴-1e⁻→CI⁺⁵ 1
CI⁺⁴+1e⁻ окислитель
CI⁺⁴-1e⁻ восстановитель
2CIO₂+2NaOH=NaCIO₂+NaCIO₃+H₂O
в) Co⁺³(OH)₃+HCI⁻¹→Co⁺²CI₂+CI₂⁰+H₂O
Co⁺³+1e⁻→Co⁺² 1 2
2
2CI⁻¹-2xe⁻→CI₂⁰ 2 1
Co⁺³ окислитель
CI⁻¹ восстановитель
2Co(OH)₃+6HCI=2CoCI₂+CI₂+6H₂O
г) I₂⁰+HN⁺⁵O₃→HI⁺⁵O₃+N⁺²O+H₂O
2I⁰-2х5e⁻→2I⁺⁵ 10 3
30
N⁺⁵+3e⁻→N⁺² 3 10
I⁰ восстановитель
N⁺⁵окислитель
3I₂+10HNO₃→6HIO₃+10NO+2H₂O
д) Zn⁰+H₂S⁺⁶O₄→Zn²⁺SO₄+S⁰+H₂O
Zn⁰-2e⁻→Zn²⁺ 2 3
6
S⁺⁶+6e⁻→S⁰ 6 1
Zn⁰ восстановитель
S⁺⁶ окислитель
3Zn+4H₂SO₄=3ZnSO₄+S+4H₂O
е) Cu₂⁻¹S⁻²+KCI⁺⁵O₃→Cu⁺²O+S⁺⁴O₂+KCI⁻¹
2Cu⁻¹-2e⁻→Cu⁺² 2 3
S⁻²-6e⁻→S⁺⁴ 6 3
CI⁺⁵+6e⁻→CI⁻¹ 6 4
Cu⁻¹ восстановитель
S⁻² восстановитель
CI⁺⁵ окислитель
3Cu₂S+4KCIO₃= 6CuO+3SO₂+4KCI
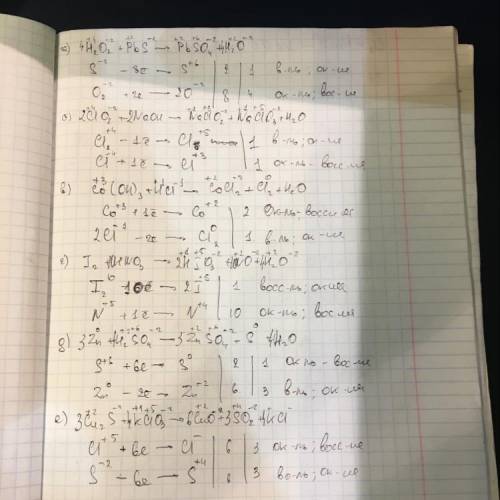
Na₂CrO₄ - в этой формуле нам известны степени окисления натрия (+1) и кислорода (-2). Исходя из этого, составим уравнение, где x - хром:
+1·2 + х·1 + (-2)·4=0
2 + x - 8 = 0
x = 8 - 2 = 6
Затем возьмём для примера хромовую кислоту - H₂⁺¹CrO₄⁻². Опять же в роли икс выступает хром:
+1·2 + х·1 + (-2)·4=0
2 + x - 8 = 0
x = 8 - 2 = 6
Далее выберем вещество, где с.о. у хрома иная. Например: гидроксид хрома (II) - Cr(OH)₂. Здесь известны с.о. водорода (+1) и кислорода (-2). Отсюда:
х·1 + 1·2 + (-2)·2 = 0
х + 2 - 4 = 0
х = 4 - 2 = 2
В общем, чтобы вычислить неизвестную степень окисления, нужно:
1. расставить известные с.о.
2. умножить их, а также х (неизвестная с.о.), на число атомов (нижний индекс)
3. вычислить х.