7.1) линейная: под действием света происходит линейная полимеризация 40%-ного водного раствора формальдегида с образованием параформа (картинка внизу).
7.2) циклическая: альдегиды самопроизвольно или под действием кислот могут вступать в реакции тримеризации и тетрамеризации, при этом образуются шести- и восьмичленные циклы с чередующимися атомами углерода и кислорода в молекуле (картинка внизу).
8) Поликонденсация: реакции поликонденсации – это процесс образования полимеров из низкомолекулярных веществ, сопровождающийся отщеплением побочных низкомолекулярных веществ – воды, спирта, галогеноводородов и т.д. Альдегиды вступают в реакцию поликонденсации с фенолом (анилином и т.д.) с образованием соответствующих полимерных смол. Реакции протекают ступенчато: сначала образуется димер, затем тример и т.д. (картинка внизу).
9) Конденсация (картинка внизу).
10) Горение: CnH2nO+O₂→nCO₂↑+nH₂O
11) Реакции окисления. Альдегиды легко окисляются до кислот даже слабыми окислителями, такими как аммиачный раствор оксида серебра (Ag₂O/NH₃, или [Ag(NH₃)₂]OH), а также свежеосажденным гидроксидом меди (II):
11.1) реакция "серебряного зеркала": R-COH+2[Ag(NH₃)₂]OH→R-COONH₄ (или RCOOH) + 2Ag↓+3NH₃↑ (или 4NH₃↑)+H₂O
Исключение для формальдегида: HCOH+4[Ag(NH₃)₂]OH→(NH₄)₂CO₃+4Ag↓+6NH₃↑+2H₂O
11.2) R-COH+2Cu(OH)₂→R-COOH+Cu₂O↓+2H₂O
12) Реакции замещения с соединениями, содержащими аминогруппу (картинка внизу).
13) Взаимодействие с пентахлоридом фосфора:
R-COH+PCl₅→R-CH-Cl+POCl₃
|
Cl
14) Замещение атома водорода в радикале в α-положении к карбонильной группе (например, галогенирование). Сильно поляризованная карбонильная группа в молекулах альдегидов и кетонов вызывает понижение электронной плотности (δ+) на атомах углерода в α-положении, вследствие чего атомы водорода приобретают повышенную реакционную и могут отщепляться в виде протона:
C2H2 Относят к алкинам Получают В лаборатории, а также в газосварочном оборудовании, ацетилен получают действием воды на карбид кальция (Ф. Вёлер, 1862 год),
а также при дегидрировании двух молекул метана при температуре свыше 1400
В промышленности ацетилен получают гидролизом карбида кальция и пиролизом углеводородного сырья — метана или пропана с бутаном. В последнем случае ацетилен получают совместно с этиленом и примесями других углеводородов. Карбидный метод позволяет получать очень чистый ацетилен, но требует высокого расхода электроэнергии. Пиролиз существенно менее энергозатратен, т.к. для нагрева реактора используется сгорание того же рабочего газа во внешнем контуре, но в газовом потоке продуктов концентрация самого ацетилена низка. Выделение и концентрирование индивидуального ацетилена в таком случае представляет сложную задачу. Экономические оценки обоих методов многочисленны, но противоречивы
1) Гидрирование (с образованием первичных спиртов):
H₃C-COH+H₂→H₃C-CH₂-OH
2) Присоединение гидросульфита натрия (только для алициклических):
H₃C-COH+NaHSO₃→H₃C-C-SO₃Na
|
OH
3) Присоединение синильной кислоты (образование гидроксинитрилов, или циангидринов): H₃C-COH+HCN→H₃C-CH-CN
|
OH
4) Присоединение спиртов (образование ацеталей):
R-COH+H₃-CH₂-OH⇄R-CH-O-CH₂-CH₃
| полуацеталь
OH
R-CH-O-CH₂-CH₃ R-CH-O-CH₂-CH₃
| +H₃C-CH₂-OH⇄ | ацеталь
OH O-CH₂-CH₃
5) Гидратация: CH₂=O+H₂O→H₂C(OH)₂ гидрат формальдегида
6) Присоединение реактива Гриньяра:
R-COH+H₃C-CH₂-MgI→R-CH-CH₂-CH₃
|
O-MgI
R-CH-CH₂-CH₃ R-CH-CH₂-CH₃
| +H₂O→ | +Mg(OH)I
O-MgI OH
7) Полимеризация (циклическая и линейная)
7.1) линейная: под действием света происходит линейная полимеризация 40%-ного водного раствора формальдегида с образованием параформа (картинка внизу).
7.2) циклическая: альдегиды самопроизвольно или под действием кислот могут вступать в реакции тримеризации и тетрамеризации, при этом образуются шести- и восьмичленные циклы с чередующимися атомами углерода и кислорода в молекуле (картинка внизу).
8) Поликонденсация: реакции поликонденсации – это процесс образования полимеров из низкомолекулярных веществ, сопровождающийся отщеплением побочных низкомолекулярных веществ – воды, спирта, галогеноводородов и т.д. Альдегиды вступают в реакцию поликонденсации с фенолом (анилином и т.д.) с образованием соответствующих полимерных смол. Реакции протекают ступенчато: сначала образуется димер, затем тример и т.д. (картинка внизу).
9) Конденсация (картинка внизу).
10) Горение: CnH2nO+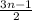 O₂→nCO₂↑+nH₂O
O₂→nCO₂↑+nH₂O
11) Реакции окисления. Альдегиды легко окисляются до кислот даже слабыми окислителями, такими как аммиачный раствор оксида серебра (Ag₂O/NH₃, или [Ag(NH₃)₂]OH), а также свежеосажденным гидроксидом меди (II):
11.1) реакция "серебряного зеркала": R-COH+2[Ag(NH₃)₂]OH→R-COONH₄ (или RCOOH) + 2Ag↓+3NH₃↑ (или 4NH₃↑)+H₂O
Исключение для формальдегида: HCOH+4[Ag(NH₃)₂]OH→(NH₄)₂CO₃+4Ag↓+6NH₃↑+2H₂O
11.2) R-COH+2Cu(OH)₂→R-COOH+Cu₂O↓+2H₂O
12) Реакции замещения с соединениями, содержащими аминогруппу (картинка внизу).
13) Взаимодействие с пентахлоридом фосфора:
R-COH+PCl₅→R-CH-Cl+POCl₃
|
Cl
14) Замещение атома водорода в радикале в α-положении к карбонильной группе (например, галогенирование). Сильно поляризованная карбонильная группа в молекулах альдегидов и кетонов вызывает понижение электронной плотности (δ+) на атомах углерода в α-положении, вследствие чего атомы водорода приобретают повышенную реакционную и могут отщепляться в виде протона:
H₃C-CH₂-CH₂-COH+Br₂→H₃C-CH₂-CH-COH+HBr
|
Br