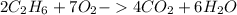
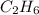 :
: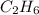 ) = 3 (г)
) = 3 (г)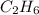 ) = 2 (моль)
) = 2 (моль)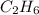 ) = 2*12+1*6 = 30 (г/моль)
) = 2*12+1*6 = 30 (г/моль)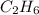 ) = 30*2 = 60 (г).
) = 30*2 = 60 (г). :
: ) = x (г)
) = x (г) ) = 4 (моль)
) = 4 (моль) ) = 12+2*16 = 44 (г/моль)
) = 12+2*16 = 44 (г/моль) ) = 44*4 = 176 (г)
) = 44*4 = 176 (г) :
: ) = y (г)
) = y (г) ) = 6 (моль)
) = 6 (моль) ) = 1*2+16 = 18 (г/моль)
) = 1*2+16 = 18 (г/моль) ) = 18*6 = 108 (г)
) = 18*6 = 108 (г) и
и  выделилось во время реакции. Для этого составляем пропорции:
выделилось во время реакции. Для этого составляем пропорции: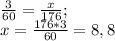 (г) - углекислого газа.
(г) - углекислого газа.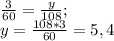 (г) - воды.
(г) - воды.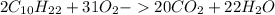
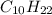 ) = 5 (г)
) = 5 (г)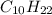 ) = 2 (моль)
) = 2 (моль)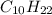 ) = 10*12+1*22 = 142 (г/моль)
) = 10*12+1*22 = 142 (г/моль)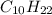 ) = 142*2 = 284 (г).
) = 142*2 = 284 (г). :
: ) = x (г)
) = x (г) ) = 20 (моль)
) = 20 (моль) ) = 12+2*16 = 44 (г/моль)
) = 12+2*16 = 44 (г/моль) ) = 44*20 = 880 (г)
) = 44*20 = 880 (г) :
: ) = y (г)
) = y (г) ) = 22 (моль)
) = 22 (моль) ) = 1*2+16 = 18 (г/моль)
) = 1*2+16 = 18 (г/моль) ) = 18*22 = 396 (г)
) = 18*22 = 396 (г)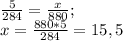 (г) - углекислого газа.
(г) - углекислого газа.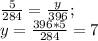 (г) - воды.
(г) - воды.
ответ:
1)дано:
cm = 0,01 м
naj
найти: [na(+)]
решение:
naj = na[+] + j[-]
1 моль данной соли образует 1 моль [na(+)] и 1 моль [j(-)]
[na(+)] = [j(-)] = 0,01 моль\л
m(naj) = cm∙ v ∙ m = 150г\моль ∙0,01моль\л ∙ 1л = 1,5г
с = 1,5г\1л = 1,5 г\л
ответ: cm [na(+)] = 0,01 моль\л
с[na(+)] = 1,5 г\л
2)дано:
кд = 4,5∙10^-7.
cm = 0,02 м
раствор н2со3
найти: [h(+)]
решение:
h2co3 = h(+) + hco3(-)
кд = [h(+)]∙[hco3(- = 4,5∙10^-7
пусть [h(+)] = х, тогда и [hco3(-)] = х, а концентрация недиссоциированных молекул:
[h2co3] = 0,02-х
х∙х\0,02-х = 4,5∙10^-7 (перерешай сам)
х = 4,5∙10^-7
3)дано:
w(na2соз) = 0,106%
р(na2соз) = 1 г/мл
найти: cm
решение:
определяем массу na2соз в растворе объемом 1 л с массовой долей 0,106%:
m(na2соз) = v ∙ р ∙ w = 1000∙1 ∙0,00106 = 1,06 г
вычисляем n(na2соз), то есть молярность раствора (vр-ра = 1 л, поэтому n(na2соз) = m(na2соз))
сm = m(na2соз)\vр-ра(na2соз) ∙ mр-ра(na2соз) = 1,06г\1 г/мл ∙ 106г\моль= 0,01m
ответ: cm = 0,01 м
5)дано:
пр(сaf2) = 4• 10^(-11)
найти: s
решение:
сaf2 = ca[2+] + 2f[-]
ca[2+] = 2f[-] = 4• 10^(-11)
молярная растворимость s
ca[2+] = s моль/л
f[-] = 2s моль/л
пр(сaf2) = ca[2+] ∙f[-]^2 = s ∙ (2s) ^2 = 4s^3
s = ( пр / 4 )1/3 = ( 4∙10-11 / 4 )1/3 = 0,00022 моль/л
ответ: s = 0,00022 моль/л или 2,2 ∙10^4
может быть