Запишем возможные уравнения реакций:
2KOH + H₂S = K₂S + 2H₂O
или:
KOH + H₂S = KHS + H₂O
Рассчитаем количество вещества гидроксида калия и сероводорода:
n (KOH) = ω*m (р-ра) / M = 0,2*560 г/56 г/моль = 2 моль
n (H₂S) = V/Vm = 1,12 л/22,4 л/моль = 0,02 моль
Явный избыток щелочи, поэтому реакция будет протекать с образование средней соли - сульфида калия: K₂S. Дальнейшие действия делаем относительно вещества взятого в недостатке.
По уравнению реакции:
n (K₂S) = n (H₂S) = 0,02 моль
ответ: образуется средняя соль - сульфид калия, количеством вещества 0,02 моль
Объяснение:
1) K2CO3 + 2HCl = 2KCl + CO2 + H2O
n(HCl) = =
= 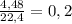 моль
моль
n(HCl) : n(CO2) = 2:1
n(CO2) = моль
моль
V(CO2) = n*Vm = 0,1 * 22,4 = 2,24 л
ответ: 2,24
2) 2K + S = K2S
n(K) = =
=  моль
моль
n(K) : n(S) = 2:1
n(S) = моль
моль
m(S) = n * M = 0,085 * 32 = 2,72 г
m(K2S) = m(K) + m(S) = 2,72 + 6,78 = 9,5 г
ответ: 9,5