Объяснение:
Даны окислительно-восстановительные реакции:
Fe + H2SO4 ® Fe2(SO4)3 + SO2 + H2O
Напишите электронные схемы, расставьте коэффициенты.
0 +1 +2 0
Fe + H2SO4 = FeSO4 + H2↑
Fe⁰ - 2e = Fe⁺² окисление, Fe⁰ - восстановитель ║1
2H⁺ + 2e = H⁰₂ восстановление, 2H⁺ - окислитель ║1
0 +6 +3 +4
2Fe + 6H2SO4(к) = Fe2(SO4)3 + 3SO2 + 6H2O
2Fe⁰ - 6e = 2Fe⁺³окисление, Fe⁰ - восстановитель ║1
S⁺⁶ + 2e = S⁺⁴восстановление, H2SO4(к) - окислитель ║3
Объяснение:
У промисловості зазвичай кисень отримують з повітря. Спочатку повітря очищають від пилу, вуглекислого газу і водяної пари, після чого зріджують при стисненні і охолодженні до 200 ° C. Рідке повітря являє собою суміш в основному азоту і кисню. Рідкий азот починає випаровуватися при більш низькій температурі (-196 ° C), ніж кисень (-183 ° C). Тому, якщо повільно нагрівати рідке повітря, то азот починає випаровуватися раніше, а кисень залишається в рідкому стані. Процеси скраплення і випаровування повторюють безліч разів, в результаті чого азот і кисень вдається розділити. Кисень і інші гази зберігають у спеціальних посудинах з подвійними стінками, між якими знаходиться вакуум
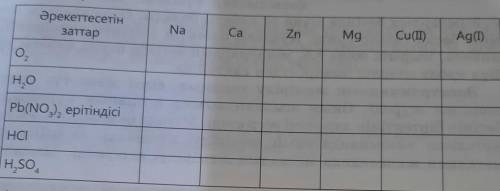
Объяснение:
2Na + O2 = Na2O2
2Ca + O2 = 2CaO
2Zn + O2 = 2ZnO
2Mg + O2 = 2MgO
2Cu + O2 = 2CuO
4Ag + O2 = 2Ag2O
2Na + 2H2O = 2NaOH + H2
Ca + 2H2O = Ca(OH)2 + H2
Zn + H2O = ZnO + H2
Mg + 2H2O = Mg(OH)2 + H2
Cu + H2O = реакция не идёт
Ag + H2O = реакция не идёт
2Na + Pb(NO3)2 = 2NaNO3 + Pb
Ca + Pb(NO3)2 = Ca(NO3)2 + Pb
Zn + Pb(NO3)2 =Zn(NO3)2 + Pb
Mg + Pb(NO3)2 = Mg(NO3)2 + Pb
Cu + Pb(NO3)2 = реакция не идёт
Ag + Pb(NO3)2 = реакция не идёт
2Na + 2HCl = 2NaCl + H2
Ca + 2HCl = CaCl2 + H2
Zn + 2HCl = ZnCl2 + H2
Mg + 2HCl = MgCl2 + H2
Cu + HCl = реакция не идёт
Ag + HCl = реакция не идёт
Na + H2SO4 = Na2SO4 + H2
Ca + H2SO4 = CaSO4 + H2
Zn + H2SO4 = ZnSO4 + H2
Mg + H2SO4 = MgSO4 + H2
Cu + H2SO4(р) = реакция не идёт
Ag + H2SO4 (р) = реакция не идёт