Начнем - с.
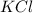 - соль сильного основания - KOH, и сильной кислоты - HCl - гидролизу не подвергается.
- соль сильного основания - KOH, и сильной кислоты - HCl - гидролизу не подвергается.
 - соль сильного основания - KOH, и слабой кислоты -
- соль сильного основания - KOH, и слабой кислоты - 
Гидролиз пойдет по аниону - 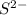
1 - ступень:
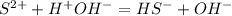 Гидроксид - аноины говорят нам о том, что среда - щелочная - лакмус синий
Гидроксид - аноины говорят нам о том, что среда - щелочная - лакмус синий
Молекулярный Вид: 
2 - ступень:
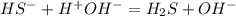 - снова щелочная среда, лакмус - синий
- снова щелочная среда, лакмус - синий
Молекулярный вид: 
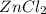 - соль слабого основания -
- соль слабого основания - 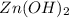 , сильной кислоты - HCl
, сильной кислоты - HCl
гидролиз пойдет по катиону - 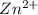
1 - ступень:
 <- катионы водорода говорят нам о том, что среда раствора кислая, лакмус - красный.
<- катионы водорода говорят нам о том, что среда раствора кислая, лакмус - красный.
МВ: 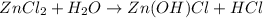
2 - ступень:
 <- снова катиончики водорода говорят нам о том, что среда кислая, а лакмус краснеет.
<- снова катиончики водорода говорят нам о том, что среда кислая, а лакмус краснеет.
МВ: 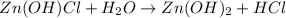
 - соль слабого основания, сильной кислоты - гидолизируется по катиону:
- соль слабого основания, сильной кислоты - гидолизируется по катиону:
1 - ступень:
 <- катионы водорода, говорят нам о том, что среда кислая, лакмус - красный.
<- катионы водорода, говорят нам о том, что среда кислая, лакмус - красный.
МВ: 
2 - ступень:
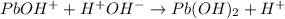 <- среда кислая, лакмус - красный
<- среда кислая, лакмус - красный
МВ: 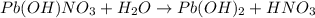
 - соль сильного основания, слабой кислоты, гидролиз по аниону.
- соль сильного основания, слабой кислоты, гидролиз по аниону.
1 - ступень:
 среда щелочная, лакмус синий
среда щелочная, лакмус синий
МВ: 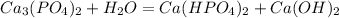
2 - ступень:
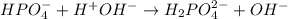
МВ: 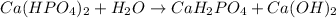
3 - ступень:

МВ: 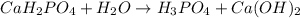 среда щелочная, лакмус синий
среда щелочная, лакмус синий
 - соль сильного основания, слабой кислоты - гидролиз по аниону.
- соль сильного основания, слабой кислоты - гидролиз по аниону.
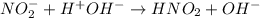 <- гидроксид - анионы угазывают на щелочной характер среды, лакмус синеет.
<- гидроксид - анионы угазывают на щелочной характер среды, лакмус синеет.
МВ: 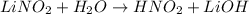
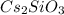 - соль сильного основания, слабой кислоты, гидролиз по аниону:
- соль сильного основания, слабой кислоты, гидролиз по аниону:
1 - ступень:
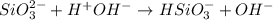 <- снова среда щелочная, лакмус синий
<- снова среда щелочная, лакмус синий
МВ: 
2 ступень:
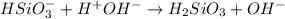
МВ: 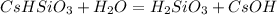
 - соль сильной кислоты, слабого основания, гидролиз по катиону:
- соль сильной кислоты, слабого основания, гидролиз по катиону:
1 - ступень:
 среда кислая, лакмус красный
среда кислая, лакмус красный
МВ: 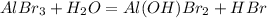
2 - ступень:
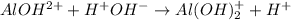
МВ: 
3 - ступень

МВ: 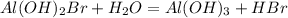
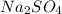 - соль сильного основания, сильной кислоты - гидролизу не подвергается, среда - нейтральная, лакмус - фиолетовый
- соль сильного основания, сильной кислоты - гидролизу не подвергается, среда - нейтральная, лакмус - фиолетовый
ответ:
сера (лат. sulfur), s, элемент с атомным номером 16, атомная масса 32,066. символ серы s произносится «эс». природная сера состоит из четырех стабильных нуклидов: 32s (содержание 95,084% по массе), 33s (0,74 %), 34s (4,16%) и 36s (0,016 %). радиус атома серы 0,104 нм. радиусы ионов: иона s2– 0,170 нм (координационное число 6), иона s4+ 0,051 нм (координационное число 6) и иона s6+ 0,026 нм (координационное число 4). энергии последовательной ионизации нейтрального атома серы от s0 до s6+ равны, соответственно, 10,36, 23,35, 34,8, 47,3, 72,5 и 88,0 эв. сера расположена в via группе периодической системы д. и. менделеева, в 3-м периоде, и принадлежит к числу халькогенов. конфигурация внешнего электронного слоя 3s23p4. наиболее характерны степени окисления в соединениях –2, +4, +6 (валентности соответственно ii, iv и vi). значение электроотрицательности серы по полингу 2,6. сера относится к числу неметаллов.
в свободном виде сера представляет собой желтые хрупкие кристаллы или желтый порошок.
в природе постепенно происходит круговорот серы, подобный круговороту азота и углерода. растения потребляют серу — ведь её атомы входят в состав белка. растения берут серу из растворимых сульфатов, а гнилостные бактерии превращают серу белков в сероводород (отсюда — отвратительный запах гниения).
но есть так называемые серобактерии,