Так, сначала я расскажу как я решал задачу, а потом оформление:
Сначала введем обозначения:
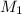 - масса раствора до добавления.
- масса раствора до добавления.
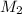 - масса раствора после добавления(соответственно)
- масса раствора после добавления(соответственно)
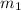 - масса соли в первом растворе
- масса соли в первом растворе
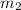 - масса соли в получившемся растворе.
- масса соли в получившемся растворе.
Исходное состояние.
Рассчитаем массу соли в исходном растворе.
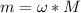 = 0,15*350г = 52,5грамма.
= 0,15*350г = 52,5грамма.
Смешиваем.
Мы добавили к первоначальному растовру 20 грамм соли - значит мы увеличили массу раствора на 20грамм, т.е. масса получившегося раствора равна: 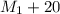 г = 350г+20г = 370грамм
г = 350г+20г = 370грамм
Но, добавив 20 грамм соли к раствору, мы увеличили не только массу арствора, но и массу соли которая есть в растворе, масса соли в получившемся растворе - 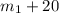 грамм = 72,5 грамм.
грамм = 72,5 грамм.
Теперь у нас есть все, чтобы рассчитать массовую долю соли в получившемся растворе: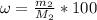 = 72,5г/370г*100% = 19,6%
= 72,5г/370г*100% = 19,6%
Теперь оформление:
Дано:
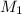 = 350г
= 350г
масса добавленной соли = 20 грамм.
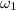 = 15%(или 0,15)
= 15%(или 0,15)
Найти:
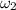 = ?
= ?
Рассчитаем массу соли в растворе:
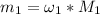 = 0,15*350г = 52,5г
= 0,15*350г = 52,5г
Рассчитаем массу получившегося расвтора:
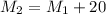 г = 350г + 20г = 370грамм
г = 350г + 20г = 370грамм
Рассчитаем массу соли в получившемся растворе: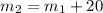 г = 52,5г + 20г = 72,5
г = 52,5г + 20г = 72,5
Рассчитываем массовую долю:
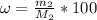 = 72,5г/370г*100% = 19,6%
= 72,5г/370г*100% = 19,6%
ответе: массовая доля соли = 19,6%(или0,196)
соотношение количеств веществ, участвующих в реакции
коэффициенты в уравнении реакции показывают не только число молекул каждого вещества, но и соотношение количеств веществ, участвующих в реакции. так, по уравнению реакции: 2h2 + o2 = 2h2o – можно утверждать, что для образования определенного количества воды (например, 2 моль) необходимо столько же моль простого вещества водорода (2 моль) и в два раза меньше моль простого вещества кислорода (1 моль). примеры подобных расчетов.
1. определим количество вещества кислорода, образующегося в результате разложения 4 моль воды.
алгоритм решения :
1. составить уравнение реакции
2. составить пропорцию, определив количества веществ по уравнению реакции и по условию (обозначить неизвестное количество вещества за х моль).
3. составить уравнение (из пропорции).
4. решить уравнение, найти х.
рис. 1. оформление краткого условия и решения 1
2. какое количество кислорода потребуется для полного сжигания 3 моль меди?
воспользуемся алгоритмом решения с использованием уравнения реакции.
рис. 2. оформление краткого условия и решения 2.
i. используя алгоритм, решите самостоятельно следующие :
1. вычислите количество вещества оксида алюминия, образовавшегося в результате взаимодействия алюминия количеством вещества 0,27 моль с достаточным количеством кислорода (4al +3o2=2al2o3).
2. вычислите количество вещества оксида натрия, образовавшегося в результате взаимодействия натрия количеством вещества 2,3 моль с достаточным количеством кислорода (4na+o2=2na2o).
алгоритм №1
вычисление количества вещества по известному количеству вещества, участвующего в реакции.
пример. вычислите количество вещества кислорода, выделившегося в результате разложения воды количеством вещества 6 моль.