ответ на фото)))))))))))))))))
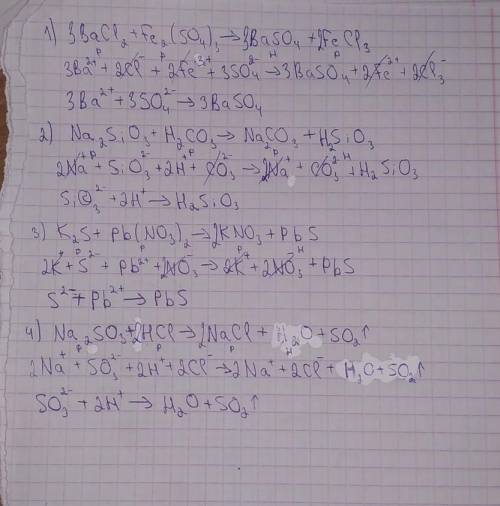
1)Cu кристаллическая решетка металлическая в узлах решетки атом-ионы.
связь - металлическая .Физическаие св-ва электро и теплопроводность металлическаий блеск .Химические св-ва Металлические
2)Cl2 кристаллическая решетка молекулярна , в узлах решетки молекулысвязь ковалентная неполярная .Физические св-ва малые температуры плавления , кипения.Обладает большой Э.О следовательно проявляет резкие НЕметаллические св-ва
3)H2 кристаллическая решетка молекулярная ,несмотря на то, что атомы внутри молекул связаны прочными ковалентными связями, между самими молекулами действуют слабые силы межмолекулярного взаимодействия.
Физические св-ва
водород-самый легкий газ имеющий низкие температуры плавления и кипения
Химические св-ва
при обычных температурах водород реагирует только с очень активными металлами
Прежде всего, нужно исходить из определения основ. Основания - сложные вещества, в состав которых входит гидроксильная группа OH⁻
и катион-металл.
Поэтому в составе любого основания имеются - группа OH и металл.
Другое - сколько гидроксильных групп приходится на один катион-металла. Это может быть одна группа, может две, может и три. Также отличием является отщеплять гидроксильную группу - это будет указывать на силу основания, сильные основания легко отдают свои группы OH в водных растворах. Отсюда также растворяться в воде. Растворимые в воде основания принято называть щелочами.
Объяснение:
1) 3BaCl2+Fe2(SO4)3=3BaSO4+2FeCl3
3Ba²⁺+6Cl⁻+2Fe³⁺+3SO4²⁻=3BaSO4+2Fe³⁺+6Cl⁻
Ba²⁺+SO4²⁻=BaSO4
2) Na2SiO3+H2CO3=Na2CO3+H2SiO3
2Na⁺+SiO3²⁻+H2CO3=2Na⁺+CO3²⁻+H2SiO3
SiO3²⁻+H2CO3=CO3²⁻+H2SiO3
3)K2S+Pb(NO3)2=2KNO3+PbS
2K⁺+S²⁻+Pb²⁺+2NO3⁻=2K⁺+2NO3⁻+PbS
S²⁻+Pb²⁺=PbS
4) Na2SO3+2HCl=2NaCl+H2O+SO2
2Na⁺+SO3²⁻+2H⁺+2Cl⁻=2Na⁺+2Cl⁻+H2O+SO2
SO3²⁻+2H⁺=H2O+SO2
Объяснение: