Задача №1
- Уравнение:
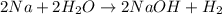
- вычислим количество вещества водорода:
n = V/Vm = 4,48л/22,4л/моль = 0,2 моль
- По уравнению реакции:
n(Na) = 2n(H2) = 0.2моль*2 = 0,4 моль
- Вычисляем массу натрия:
m(Na) = n*M = 0,4моль*23г/моль = 9,2 грамма
Отвеот: масса натрия равна 9,2 грамма
Задача №2
- Уравнение:
CuO + H2 = Cu + H2O
-По уравнению реакции, видим, что:
n(H2) = n(CuO) = 1,5 моль
- Масса 1,5 моль водорода:
m= n*M = 2г/моль*1,5моль = 3 грамма
- По уравнению реакции, видим, что:
n(Cu) = n(CuO) = 1.5 моль
- Рассчитывеам массу 1,5 моль меди:
m = n*M = 1,5 моль*64г/моль = 96 грамм
Объяснение:
CaI2 Ca(+2)I(-)
BaO Ba(+2)O(-2)
B2S3 B(+3)S(-2)
CO2 C(+4)O(-2)
CrO3 Cr(+6)O(-2)
NH3 N(-3)H(+)
F2 F(0)
K2SiO3 K(+)Si(+4)O(-2)
NaOH Na(+)O(-2)H(+)
Al(NO3)3 Al(+3)N(+5)O(-2)
LiH Li(+)H(-)
3) Mr(Al(NO3)3 = 27 + 14*3 + 16*9 = 213
W(Al) = Ar(Al) *n / Mr(Al(NO3)3 *100% = 27*1 / 213 *100% = 13%
W(N) = Ar(N) *n / Mr(Al(NO3)3) *100% = 14*3 / 213 *100% = 20%
W(O) = Ar(O) *n / Mr(Al(NO3)3 *100% = 16*9 / 213 *100% = 67%