Zn + H2SO4 = ZnSO4 + H2
пропорция
3/65 = Х/22,4
Х = 3*22,4/65 = 1,034 л - объем выделившегося водорода.
 (оксид магния)
(оксид магния) 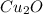 (оксид меди)
(оксид меди) 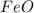 (оксид железа (II))
(оксид железа (II)) 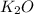 (оксид калия)
(оксид калия) 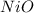 (оксид никеля(II))
(оксид никеля(II))  (оксид натрия)
(оксид натрия) 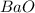 (оксид бария)
(оксид бария)  (гидроксид магния)
(гидроксид магния)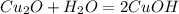 (гидроксид меди)
(гидроксид меди)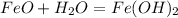 (гидроксид железа (II))
(гидроксид железа (II))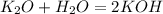 (гидроксид калия)
(гидроксид калия)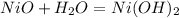 (гидроксид никеля(II))
(гидроксид никеля(II)) (гидроксид натрия)
(гидроксид натрия)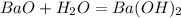 (гидроксид бария)
(гидроксид бария) 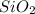 (оксид кремня (IV))
(оксид кремня (IV))  (оксид хрома (VI))
(оксид хрома (VI)) 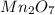 (оксид марганца (VII))
(оксид марганца (VII))  (оксид серы (IV))
(оксид серы (IV)) 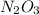 (оксид азота (III))
(оксид азота (III))  (оксид азота (II))
(оксид азота (II))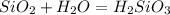 (кремниевая кислота)
(кремниевая кислота)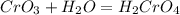 (хромовая кислота)
(хромовая кислота)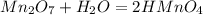 (марганцевая кислота)
(марганцевая кислота)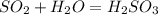 (сернистая кислота)
(сернистая кислота) (азотистая кислота)
(азотистая кислота)  (азотистая кислота)
(азотистая кислота)
Основные оксиды: соединения металла с кислородом
Fe⁺²O⁻² (оксид железа (II)), его основание Fe⁺²(O⁻²H⁺)₂ (гидроксид железа (II))
Cu₂⁺O⁻² (оксид меди (I)), его основание Cu⁺O⁻²H⁺ (гидроксид меди (I))
Cs₂⁺O⁻² (оксид цезия), его основание Cs⁺O⁻²H⁺ (гидроксид цезия)
Кислотные оксиды: соединения неметалла и кислорода
Cl₂⁺⁷O₇⁻² (оксид хлора (VII)), его кислота H⁺Cl⁺⁷O₄⁻² (хлорная кислота)
S⁺⁶O₃⁻² (оксид серы (VI)), его кислота H₂⁺S⁺⁶O₄⁻² (серная кислота)
Про остальное:
H⁺Cl⁻ - хлороводородная кислота (бескислородная, поэтому своего оксида у нее нет)
K⁺O⁻²H⁺ - гидроксид калия, имеет свой основный оксид K₂⁺O⁻² (оксид калия)
H₂O - вода, не относится ни к кислотным, ни к основным, ни к амфотерным оксидам, хоть и проявляет себя как ОЧЕНЬ слабая кислота и ОЧЕНЬ слабое основание
Fe⁺³Cl₃⁻ - соль хлорид железа (III)
Ca⁺²(O⁻²H⁺)₂ - гидроксид кальция, имеет свой основный оксид Ca⁺²O⁻² (оксид кальция)
H₂SO₄ - серная кислота, о ней было выше в кислотных оксидах
Zn + H2SO4 => ZnSO4 + H2
m 3г
n(Zn)=== 0,046моль
M 65г/моль
по уравнению n(Zn) =n(H2) = 0,046 моль
V (H2) = Vm * n = 22,4 л/моль * 0,046 моль= 1,03 л