ответ:Дано: м аса раствора m (р-на) = 300 г, w (г.г..) = 30%
Найти: m (г.г..) - ?, M (растворителя) -?
И Из формулы W (г.г..) = (M (г.г..) / M (р-на)) ∙ 100% найдем массу растворенного вещества.
m (г.г..) = (W (г.г.) ∙ m (р-на)) 100% = (30 ∙ 300 г): 100% = 90 г.
Найдем массу растворителя в растворе:
m (растворителя ) = m (р-на) - m (г.г..) = 300 г - 90 г = 210 г
ИИ образом.
Составим пропорцию и решим ее для вычисления массы растворенного вещества.
То, что массовая доля растворенного вещества равна 30% означает, что
в 100 г раствора содержится 30 г растворенного вещества, тогда
в 300 г раствора будет содержаться х г растворенного вещества.
100 г / 300 г = 30 г / х г, отсюда
х = 30 г • 300 г / 100 г = 90 г.
Найдем массу растворителя в растворе:
m (растворителя) = m (р-на) - m (г.г..) = 300 г - 90 г = 210 г
ответ: для приготовления раствора 300 г с массовой долей растворенного вещества 30% нужно взять 90 г растворенного вещества и растворитель массой 210 г.
Объяснение:
S - сера
Сера в самородном состоянии, а также в виде сернистых соединений известна с древнейших времён. Элементарную природу серы установил Лавуазье в опытах по сжиганию
3 малый период, VI группа, главная подгруппа.
(Электронно-графическая формула в фото 1)
Степень окисления: -2, 0, +4,+6
Валентность: IV, VI
Высший оксид: SO3, летучее водородное соединение: H2S
Неметалл
Нахождение в природе:
- в самородном виде:
Cера встречается в природе в свободном (самородном) состоянии, поэтому она была известна человеку уже в глубокой древности.
- в виде соединений:
PbS – свинцовый блеск,
ZnS – цинковый блеск (цинковая обманка)
FeS2 – пирит (серный колчедан)
HgS – киноварь
Для серы характерно явление аллотропии.\
Ромбическая сера – это наиболее устойчива модификация, состоит из молекул S8. Кристаллы имеют лимонно-желтый цвет и полупрозрачны, Tпл.= 112,8 °С.
Моноклинная сера имеет вид желтых игольчатых кристаллов, Tпл.= 119,3 °С.
Пластическая сера – Вязкая тёмно-коричневая масса, которая через несколько дней снова превращается в ромбическую.
Химические свойства:
Сера в химических реакциях проявляет окислительные и восстановительные свойства.
1. Сера взаимодействует с металлами. При этом образуются соли - сульфиды:
2Al + 3S → Al2S3 (сульфид алюминия)
Cu + S → CuS (сульфид меди (II))
Hg + S → HgS (сульфид ртути (II))
2. При повышенной температуре реагирует с водородом:
S + H2→ H2S (сероводород)
3. Сера горит в кислороде голубоватым пламенем.
S + O2→ SO2 (оксид серы (IV))
4. Сера реагирует с галогенами:
S + 3F2 → SF6
Основные отрасли применения:
- для производства серной кислоты
- для производства бенгальских огней
- для производства бумаги
- Изготовление веществ для удобрения растений.
- Получения цветных металлов.- Для придачи стали дополнительных свойств.- Для изготовления спичек, материалов для взрывов и пиротехники.- Для производства краски, волокон - Для отбеливания ткани.получение:самородную серу добывают непосредственно из пластов в недрах земли. Ее потом очищают разными методами.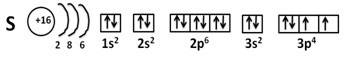
Объяснение:
Надеюсь это то, что ты имел(а) ввиду