
Правило "рычага" для растворов (вывод ищите в учебниках по физической химии, раздел "Фазовые равновесия" двухкомпонентных систем):
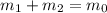
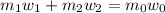
Концентрацию второго раствора находим из соотношений молярных масс соли и кристаллогидрата:
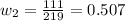
Концентрация соли в воде, очевидно, равна нулю. Следовательно, масса второго раствора будет равна:
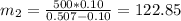 г.
г.
Масса чистой соли во втором растворе:
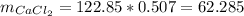 г.
г.
Количество вещества соли:
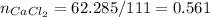 моль.
моль.
Объём второго раствора:
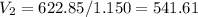 мл (0.542 л)
мл (0.542 л)
Отсюда находим молярность и нормальность раствора (фактор эквивалентности хлорида кальция равен 1/2):
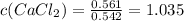 моль/л. [Молярность]
моль/л. [Молярность]
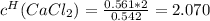 моль-экв/л. [Нормальность]
моль-экв/л. [Нормальность]
НВr - ковалентная полярная связь (между неметаллом и неметаллом с разной электроотрицательностью). У водорода и брома образуется одна общая электронная пара, отсюда связь одинарная, схема, вроде выглядит так: Н-Br. Электронная пара смещена к брому (так как бром наиболее электроотрицателен).
СО2 - также ковалентная полярная связь. Образуется двойная связь: О=С=О. Электронные пары смещены к атомам кислорода (так как кислород наиболее электроотрицателен).
FeS - ионная связь (между металлом и неметаллом, проще говоря атомы металлов отдают свои электроны с внешнего энергетического уровня, образуя ионы (катионы - положительно заряженные ионы), а неметаллы эти электроны принимают, чтобы завершить внешний энергетический уровень (собрать на нем 8 электронов), также образуя ионы (анионы - отрицательно заряженные ионы).
Я так и не поняла как здесь написать заряд иона, поэтому буду писать в скобках, а так пишется на месте показателя степени.
Fe(0) - 2е → Fe(+2)
S(0) + 2e → S(-2)
Fe(0) + S(0) → Fe(+2) + S(-2) →FeS
Мы всегда делали так, если что непонятно, спрашивай)