ответ:
если равновесная концентрация кислорода стала 0.05 моль/л, то значит в реакцию вступило 0.1 - 0.05 = 0.05 моль кислорода
по уравнению реакции столько же вступило и азота
значит равновесная концентрация азота 0.3 - 0.05 = 0.25 моль/л
по уравнению реакции образовалось вдвое больше оксида азота
значит равновесная концентрация оксида азота 0.05 * 2 = 0.1
обобщенная схема будет выглядеть так
считаем константу равновесия
так как сумма коэффициентов в левой части уравнения = сумме коэффициентов в правой, то изменение давления никак не повлияет на смещение равновесия
подробнее - на -
объяснение:
Это уравнение как для ОВР не простое, так как степень окисления железа в 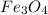 равна
равна 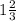 :
:
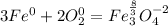
Так что рассмотрим сложный оксид 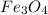 как сумму двух
как сумму двух 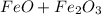
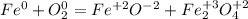
Рассмотрим процессы

Так как количество принятых электронов равно количеству отданных, то перед кислородом идет коэффициент 2, а перед вторым уравнением тоже идет коэффициент 2:
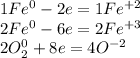
Получается суммарно 3 атома железа отдали 8 электронов и 4 атома кислорода приняли 8 электронов
Кислород - окислитель, железо - восстановитель
Тогда суммарный коэффициент перед железом 1 + 2 = 3, а перед кислородом 2, тогда:

0,70 0,18
0,33 -конверт Пирсона
0,15 0,37
m(70%)=300 :(0,18+0,37)*0,18=98,2г;
m(15%)=300 : (0,18+0,37)*0,37=201,8г.