2Mg+O₂-->2MgO
Сначала найдём количество магния по формуле n=m/M, где n-колличество вещества, m-масса, M-молярная масса:
n(Mg)=12г:24г/моль=0,5моль
Теперь смотрим на коэффициенты перед магнием и кислородом.
Перед магнием стоит 2, а перед кислородом 1.
Значит, колличество кислорода в 2 раза меньше колличества магния:
n(O₂)=n(Mg)/2=0,5моль:2=0,25моль
Теперь можем найти объём кислорода по формуле 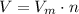
где V-объём, 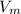 -молярный объём (у газов он всегда равен 22,4 л/моль), n-колличество вещества:
-молярный объём (у газов он всегда равен 22,4 л/моль), n-колличество вещества:
V(O₂)=22,4л/моль·0,25моль=5,6л
ответ: 5,6 л.
Для начала фраза "добавили достаточное кол-во серной кислоты" говорит нам, что можно считать что прореагировал весь хлорид бария. Теперь определим, сколько ж его вступило в реакцию. Из 40 г раствора 20,8% его массы составляет хлорид бария. Это составит 40*20,8/100=8,32 г BaCl2
Смотрим на уравение реакции: BaCl2+H2SO4=BaSO4+2HCl
Масса одного моль BaCl2 = 208 г
Масса одного моль BaSO4 = 233 г
Т.е. из 208 г хлорида бария образуется 233 г сульфата бария. В нашем случае из 8,32 г хлорида образуется 8,32*233/208 =9,32 г сульфата. Вот столько его и должно выпасть в осадок :-)
сульфит магния- MgSO3
хлорид свинца- PbCl3
карбонат берилия- BeCO3
сульфид ртути(1)- HgS
нитрат железа(2)- Fe(NO3)2
фосфат железа(1)- Fe3PO4
сульфат стронция- SrSO4
нитрат меди(1)- CuNO3