Дано:
m (бутена) = 100 %;
галоген (обозначим его Г);
m (после р.-ции) = 167,86 %.
Найти:
галоген (Г) — ?
1. Сначала напишем реакцию в общем виде (прикреплена ниже на фото).
2. Затем посчитаем молярную массу бутена. Берём значения из таблицы Менделеева.
M (C₄H₈) = 4 · 12 + 8 = 56 (г/моль).
3. Массу бутена примем за 100%, а массу галогенпроизводного будем считать за 167,86%.
Таким образом мы найдём молярную массу галогенпроизводного.
56 г/моль — 100 %
x г/моль — 167,86 %
x ≈ 94 (г/моль).
4. По уравнению реакции видим, что количество углеродов и водородов не поменялось, но теперь "висят" два радикала галогена.
Значит, от массы галогенпроизводного отнимем "бутен", чтобы у нас остались только галогены, а так как их два, разделим на 2 и узнаем молярную массу искомого галогена.
M (Г) = (94 г/моль – 56 г/моль) ÷ 2 = 19 (г/моль).
Смотрим по таблице Менделеева... это фтор (F)!
ответ: фтор (F).
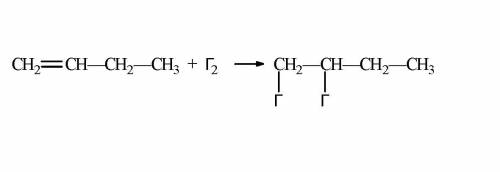
Объяснение:
Карбид алюминия массой 180 грамм, содержащий 20% примесей, растворили в серной кислоте. Выделившийся газ смешали с хлором, объемом 112 л. Вычислите объем (в литрах) получившегося хлороводорода, если выход в обоих процессах (растворение и монохлорирование) составляет 60% по массе. (Запишите число с точностью до тысячных)
Молярная масса Аl₄C₃ равна 144 г/моль. Масса чистого карбида алюминия равна 180 г × 0,8 = 144 г.
1 моль 3 моль
Аl₄C₃ + 6H₂SO₄ = 2Al₂(SO₄)₃ + 3CH₄
Выход метана по массе 60% составляет 1,8 моль
1,8 моль 5 моль 1,8 моль 1.8 моль
СН₄ + Сl2 = СН3Сl + HCl
Выход хлороводорода по массе 60% составляет 1,08 моль
V(HCl) = 22,4 л/моль × 1,08 моль = 24,192 литра.
Находим количество вещества серы: n(S) = m/M = 8 г/32 г/моль = 0,25 моль. По уравнению реакции, столько же образовалось и оксида серы. Поскольку теплота образования рассчитывается на 1 моль вещества, составим простую пропорцию:
0,25 моль SO2 73,45 кДж
1 моль SO2Х кДж
Отсюда Х= 1*73,45/0,25 = 293,8 кДж.
Одновременно это будет и теплота реакции, которая обычно записывается в уравнении:
S + O2 = SO2 + 293,8 лДж
Объяснение:
обьеснять ненадо