Fe2O3(т) + ЗСО(г) = 2Fe(т) + ЗСО2(г)
∆H -824 -110 0 -393
∆S 87 198 27 214
∆G -742 -137 0 -394
∆H=[3*-393] - [3*-110-824]=-1179+1154=-25 кДж/моль
∆S=[27*2+214*3]-[198*3+87]=696-681=15 Дж/(К*моль)
∆G=[-394*3]-[3*-137-724=]=-1182+1135=-47 кДж/моль
тк ∆G<0, то реакция невозможна при нормальной температуре. чтобы найти температуру, при которой ∆G изменит знак, приравняем ее к нулю.
∆G=∆H-T∆S из формулы получим:
T=∆H/∆S=-25000/15=1666.7К = 1393.7 С
108г хг
4P + 5O2 = 2P2O5
v=4моль v=2моль
М=31г/моль М=142г/моль
m=124г m=284г
сост. пропорцию:
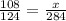
х=(284г*108г)/124г=247г
вместо пропорции можно через моль:
v(P)=108г/(31г/моль)=3,48моль
v(P2O5)=v(P):2=3,48моль:2=1,74моль(т.к.фосфор и оксид фосфора 5 относятся как 4:2=2:1.Это можно увидеть в уравнении реакции,смотря на коэффициенты перед формулами фосфора и оксида)
m(P2O5)=1,74моль*142г/моль=247г
ответ:247г
С2H4 + H2O= C2H5OH
1 моль 1 моль
2.5 мольх (2.5 моль)
n(C2H4)= m/M= 70/26 = 2.5 моль
m ( C2H5OH)= n*M= 2.5*46= 115
m теор= 115*94/100= 108.1 гр